Câu hỏi:
05/01/2024 98
Giải thích vì sao ở điều kiện thường nước ở thể lỏng, có nhiệt độ sôi cao (100oC).
Giải thích vì sao ở điều kiện thường nước ở thể lỏng, có nhiệt độ sôi cao (100oC).
A. Phân tử nước có liên kết cộng hóa trị.
A. Phân tử nước có liên kết cộng hóa trị.
B. Phân tử nước có liên kết cho – nhận.
B. Phân tử nước có liên kết cho – nhận.
C. Nhờ liên kết hydrogen.
C. Nhờ liên kết hydrogen.
D. Nhờ tương tác van der Waals.
D. Nhờ tương tác van der Waals.
Trả lời:
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án đúng là: C
Nhờ liên kết hydrogen ở điều kiện thường nước ở thể lỏng, có nhiệt độ sôi cao (100oC).
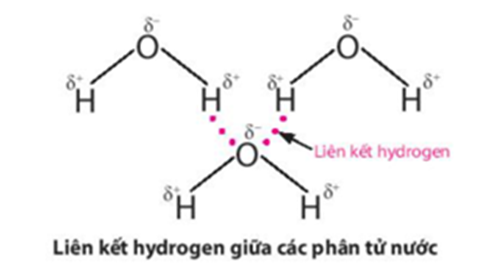
Đáp án đúng là: C
Nhờ liên kết hydrogen ở điều kiện thường nước ở thể lỏng, có nhiệt độ sôi cao (100oC).

CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 2:
Liên kết hydrogen không được hình thành giữa hai phân tử nào sau đây?
Liên kết hydrogen không được hình thành giữa hai phân tử nào sau đây?
Câu 3:
Các khí hiếm như neon, argon, … tồn tại dưới dạng các nguyên tử độc lập. Tuy nhiên ở nhiệt độ thấp, khí hiếm có thể hóa lỏng, đó là do tồn tại
Các khí hiếm như neon, argon, … tồn tại dưới dạng các nguyên tử độc lập. Tuy nhiên ở nhiệt độ thấp, khí hiếm có thể hóa lỏng, đó là do tồn tại
Câu 6:
Giải thích vì sao tính acid của HF yếu hơn rất nhiều so với các acid HCl, HBr, HI.
Giải thích vì sao tính acid của HF yếu hơn rất nhiều so với các acid HCl, HBr, HI.
Câu 7:
So với lực kiên kết ion, liên kết cộng hóa trị hay liên kết kim loại thì tương tác giữa các phân tử
So với lực kiên kết ion, liên kết cộng hóa trị hay liên kết kim loại thì tương tác giữa các phân tử
Câu 11:
Giải thích vì sao cùng là phân tử phân cực, ở nhiệt độ phòng, fluorine, chlorine là những chất khí còn bromine là chất lỏng?
Giải thích vì sao cùng là phân tử phân cực, ở nhiệt độ phòng, fluorine, chlorine là những chất khí còn bromine là chất lỏng?
Câu 13:
Liên kết hydrogen và tương tác van der Waals ảnh hưởng như thế nào đến nhiệt độ nóng chảy và nhiệt độ sôi của các chất?
Liên kết hydrogen và tương tác van der Waals ảnh hưởng như thế nào đến nhiệt độ nóng chảy và nhiệt độ sôi của các chất?


