Cấu hình electron của các ion được thiết lập bằng cách nhận hoặc nhường electron, bắt đầu từ phân lớp ngoài cùng của
461
31/05/2023
Bài 3* trang 30 Hóa học 10: Cấu hình electron của các ion được thiết lập bằng cách nhận hoặc nhường electron, bắt đầu từ phân lớp ngoài cùng của cấu hình electron nguyên tử tương ứng.
a) Viết cấu hình electron của ion Na+ và ion Cl-.
b) Nguyên tử Cl nhận 1 electron để trở thành ion Cl-, electron này xếp vào AO thuộc phân lớp nào của Cl? AO đó là AO trống, chứa 1 hay 2 electron?
Trả lời
a) Cấu hình electron của Na (Z = 11): 1s22s22p63s1. Nguyên tử Na nhường 1 electron để được ion Na+.
⇒ Cấu hình electron của Na+ là 1s22s22p6.
Cấu hình electron của Cl (Z = 17): 1s22s22p63s23p5. Nguyên tử Cl nhận 1 electron để được ion Cl‑.
⇒ Cấu hình electron của Cl- là 1s22s22p63s23p6
b) Cấu hình theo orbital lớp ngoài cùng của nguyên tử Cl
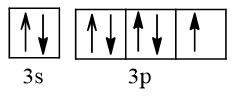
Nguyên tử Cl nhận 1 electron để trở thành ion Cl-, electron này xếp vào AO thuộc phân lớp 3p của Cl. AO đó là AO chứa 1 electron.

