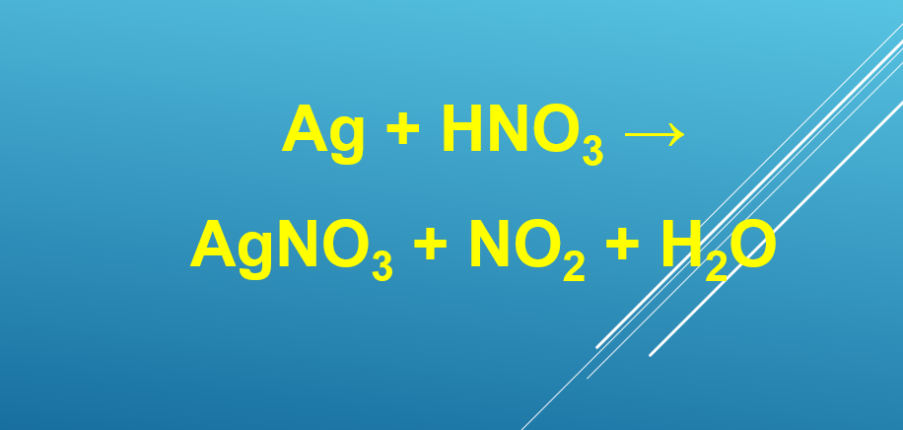
Phản ứng Ag + HNO3 → AgNO3 + NO2 + H2O
1. Phương trình phản ứng Ag + HNO3
Ag + 2HNO3 → AgNO3 + NO2 + H2O
Lưu ý: Các kim loại trung bình và yếu như Ag, Cu,....: kim loại trung bình, yếu thì có tính khử yếu, nên có khả năng khử N+5 trong HNO3 xuống N+4 tương ứng trong NO2
2. Điều kiện phản ứng Ag tác dụng HNO3 loãng xảy ra
Nhiệt độ thường
3. Bản chất của các chất tham gia phản ứng
3.1. Bản chất của Ag (Bạc)
- Trong phản ứng trên Ag là chất khử.
- Ag là kim loại quý kém hoạt động nhưng ion Ag+ có tính oxi hóa mạnh.
- Ag không tác dụng với HCl và H2SO4 loãng, nhưng tác dụng với các axit có tính oxi hóa mạnh, như HNO3 hoặc H2SO4 đặc, nóng.
3.2. Bản chất của HNO3 (Axit nitric)
- Trong phản ứng trên HNO3 là chất oxi hoá.
- Đây là một monoaxit mạnh, có tính oxi hóa mạnh có thể nitrat hóa nhiều hợp chất vô cơ.
4. Tính chất hóa học của Ag
Kém hoạt động (kim loại quý), nhưng ion Ag+ có tính oxi hóa mạnh, bạc có thế điện cực chuẩn (E0Ag+/Ag= + 0,80V).
4.1. Tác dụng với phi kim
Bạc không bị oxi hóa trong không khí dù ở nhiệt độ cao.
Tác dụng với ozon
2Ag + O3 → Ag2O + O2
4.2. Tác dụng với axit
Bạc không tác dụng với HCl và H2SO4 loãng, nhưng tác dụng với các axit có tính oxi hóa mạnh, như HNO3 hoặc H2SO4 đặc, nóng.
3Ag + 4HNO3 (loãng) → 3AgNO3 + NO + 2H2O
2Ag + 2H2SO4 (đặc, nóng) → Ag2SO4 + SO2 + 2H2O
4.3. Tác dụng với các chất khác
- Bạc có màu đen khi tiếp xúc với không khí hoặc nước có mặt hidro sunfua:
4Ag + 2H2S + O2 (kk) → 2Ag2S + 2H2O
- Bạc tác dụng được với axit HF khi có mặt của oxi già:
2Ag + 2HF (đặc) + H2O2 → 2AgF + 2H2O
2Ag + 4KCN (đặc) + H2O2 → 2K[Ag(CN)2] + 2KOH
5. Bài tập vận dụng liên quan
Câu 1. Trong phòng thí nghiệm người ta điều chế HNO3 từ
A. NH3 và O2
B. NaNO2 và H2SO4 đặc.
C. NaNO3 và H2SO4 đặc.
D. NaNO2 và HCl đặc.
Lời giải:
Câu 2. Chỉ sử dụng dung dịch HNO3 loãng, có thể nhận biết được bao nhiêu chất rắn riêng biệt sau: MgCO3, Fe3O4, CuO, Al2O3?
A. 1.
B. 2.
C. 3.
D. 4.
Lời giải:
Câu 3. HNO3 phản ứng với tất cả các chất trong nhóm nào sau đây?
A. NH3, Al2O3, Cu2S, BaSO4.
B. Cu(OH)2, BaCO3, Au, Fe2O3.
C. CuS, Pt, SO2, Ag.
D. Fe(NO3)2, S, NH4HCO3, Mg(OH)2.
Lời giải:
Câu 4. Nhận định nào sau đây là sai ?
A. HNO3 phản ứng với tất cả bazơ.
B. HNO3 (loãng, đặc, nóng) phản ứng với hầu hết kim loại trừ Au, Pt.
C. Tất cả các muối amoni khi nhiệt phân đều tạo khí amoniac.
D. Hỗn hợp muối nitrat và hợp chất hữu cơ nóng chảy có thể bốc cháy.
Lời giải:
Câu 5. Hòa tan 23,2 gam hỗn hợp X gồm Fe3O4 và CuO có cùng khối lượng vào dung dịch HNO3 vừa đủ chứa 0,77 mol HNO3 thu được bằng dung dịch Y và khí Z gồm NO và NO2. Khối lượng mol trung bình của Z bằng
A. 42.
B. 38.
C. 40,667.
D. 35,333.
Lời giải:
Câu 6. Hòa tan hết 10,8 gam Ag vào dung dịch HNO3 đặc, đun nóng thu được khí X (sản phẩm khử duy nhất). Hấp thụ toàn bộ khí X vào 200ml dung dịch KOH 1M thu được dung dịch Y. Cô cạn dung dịch Y rồi nung đến khối lượng không đổi thì khối lượng chất còn lại là (Cho Ag = 108, N = 14, O = 16, K = 39)
A. 19,94 gam
B. 8,5 gam
C. 14,1 gam
D. 19,14 gam
Lời giải:
Ag tác dụng với dung dịch HNO3 đặc, nóng thì sản phẩm khử là NO2
Ag + 2HNO3 → AgNO3 + NO2 + H2O
0,1 0,1
2NO2 + 2KOH → KNO2 + KNO3 + H2O
0,1 0,1 0,05 0,05
Sản phẩm gồm: KNO2, KNO3, KOH dư. Khi nung thì:
2KNO3 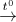 2KNO2 + O2
2KNO2 + O2
0,05 0,05
Ta thu được: KOH dư: 0,1 mol và KNO2: 0,1 mol
m = 56.0,1 + 85.0,1 = 14,1 (gam)
Câu 7. Hòa tan m gam hỗn hợp A gồm Cu, Ag trong dung dịch HNO3 thu được dung dịch B chứa hỗn hợp 7,06g muối và 0,05 mol NO2 (duy nhất). Giá trị của m là:
A. 2,2
B. 3,06
C. 2,58
D. 3,96
Lời giải:
0,05 mol NO2 đã nhận 0,05 mol e
⇒ số mol điện tích (+) tạo ra là 0,05 mol
⇒ Số mol NO3- là 0,05 mol
⇒ m = mmuối – mNO3- = 7,06 - 0,05.62 = 3,96g
Xem thêm các phương trình hóa học liên quan khác:
Ag + HNO3 → AgNO3 + NO + H2O | Ag ra AgNO3
AgNO3 → Ag + NO2 + O2 l AgNO3 ra Ag
HCHO + AgNO3 + NH3 + H2O → Ag + NH4NO3 + (NH4)2CO3 | HCHO ra NH4NO3
AgNO3 + H2O + NH3 + HCOOH → (NH4)2CO3 + Ag + NH4NO3 | AgNO3 ra Ag