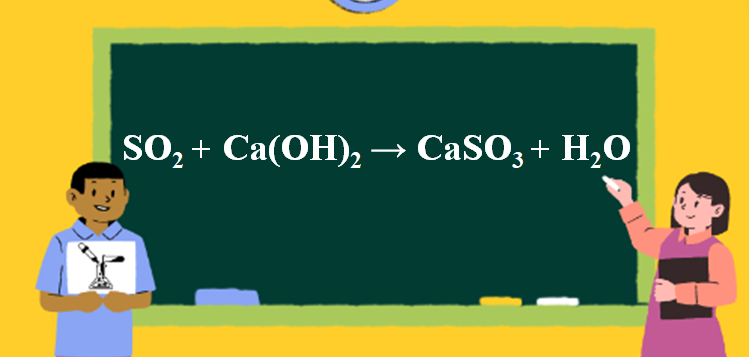Phản ứng SO2 + Ca(OH)2 → CaSO3 + H2O
1. Phương trình phản ứng SO2 ra CaSO3
SO2 + Ca(OH)2→ CaSO3+ H2O
2. Điều kiện để SO2 tác dụng Ca(OH)2
Nhiệt độ thường
SO2 sẽ tác dụng với nước vôi trong Ca(OH)2, lúc này nước vôi trong hoàn toàn vẩn đục.
3. Bản chất của các chất tham gia phản ứng
3.1. Bản chất của SO2 (Lưu huỳnh dioxit)
SO2 là oxit axit tác dụng với dung dịch bazo tạo thành muối và nước.
3.2. Bản chất của Ca(OH)2 (Canxi hidroxit)
Ca(OH)2 là một bazo mạnh phản ứng được với oxit axit.
4. Bài toán SO2 dẫn vào dung dịch Ca(OH)2
Do ta không biết sản phẩm thu được là muối nào nên phải tính tỉ lệ T:
Ca(OH)2 + SO2 → CaSO3↓ + H2O (1)
Ca(OH)2 + 2SO2 → Ca(HSO3)2 (2)
Đặt T = nSO2 : nCa(OH)2
Nếu T ≤ 1: chỉ tạo muối CaSO3
Nếu T = 2: chỉ tạo muối Ca(HSO3)2
Nếu 1 < T < 2: tạo cả muối CaSO3và Ca(HSO3)2
Hấp thụ SO2 vào nước vôi trong thấy có kết tủa, thêm NaOH dư vào thấy có kết tủa nữa suy ra có sự tạo cả CaSO3 và Ca(HSO3)2
Hấp thụ CO2vào nước vôi trong thấy có kết tủa, lọc bỏ kết tủa rồi đun nóng nước lọc lại thấy kết tủa nữa suy ra có sự tạo cả CaSO3 và Ca(HSO3)2.
5. Tính chất hoá học của SO2
* Lưu huỳnh đioxit tác dụng với nước:
SO2 + H2O ⇋ H2SO3
* Lưu huỳnh đioxit tác dụng với dung dịch bazơ (có thể tạo thành 2 loại muối sunfit và hiđrosunfit)
SO2 + NaOH → NaHSO3
SO2 + 2NaOH → Na2SO3 + H2O
* Lưu huỳnh đioxit tác dụng với oxit bazơ → muối:
SO2 + CaO → CaSO3
SO2 vừa là chất khử, vừa là chất oxi hóa (do S trong SO2 có mức oxi hóa trung gian +4)
* Lưu huỳnh đioxit là chất oxi hóa:
SO2 + 2H2S → 3S + 2H2O
Lưu huỳnh đioxit là chất khử
6. Tính chất hóa học của Ca(OH)2
Dung dịch Ca(OH)2 có có tính bazơ mạnh. Mang đầy đủ tính chất của bazơ:
Tác dụng với axit:
Ca(OH)2 + 2HCl → CaCl2 + 2H2O
Tác dụng với muối:
Ca(OH)2 + Na2CO3 → CaCO3↓ + 2NaOH
Tác dụng với oxit axit:
Ca(OH)2 + CO2 → CaCO3↓ + H2O
Chú ý: Khi sục từ từ khí CO2 tới dư vào dung dịch Ca(OH)2 thì
+ Ban đầu dung dịch vẩn đục:
Ca(OH)2 + CO2 → CaCO3↓ + H2O
+ Sau đó kết tủa tan dần và dung dịch trong suốt:
CO2 + H2O + CaCO3 → Ca(HCO3)2
7. Câu hỏi vận dụng
Câu 1. Dẫn từ từ SO2vào nước vôi trong cho đến dư, hiện tượng xảy ra là:
A. Nước vôi từ trong hóa đục, rồi lại từ đục hóa trong
B. Nước vôi từ đục hóa trong, rồi lại từ trong hóa đục
C. Nước vôi từ trong hóa đục
D. Nước vôi từ đục hóa trong
Lời giải:
Đáp án: A
Giải thích:
Ban đầu toàn bộ SO2 sẽ tác dụng với nước vôi trong Ca(OH)2, lúc này nước vôi trong hoàn toàn vẩn đục.
Ca(OH) + SO2→ CaSO3 + H2O
Nhưng vì dẫn đến dư SO2 nên toàn bộ SO2 dư sẽ tác dụng tiếp tục với dung dịch sau phản ứng tạo thành dung dịch trong suốt, không còn bị vẩn đục.
CaSO3 + H2O + SO2→ Ca(HSO3)2
Các chất còn lại cuối cùng trong dung dịch:
Ca(HSO3)2, H2O và SO2 thôi.
Câu 2. Hòa tan V lít khí SO2 (đktc) vào 100 ml dung dịch NaOH 1,2M thì thu được 10,02 gam hỗn hợp hai muối. Tìm giá trị của V
A. 2,016 lít.
B. 1,344 lít.
C. 0,672 lít.
D. 2,24 lít.
Lời giải:
Đáp án: A
Câu 3. Hấp thụ hoàn toàn 12,8 gam SO2 vào 250 ml dung dịch NaOH 1M. Khối lượng muối tạo thành sau phản ứng là
A. 15,6 gam và 5,3 gam.
B. 18 gam và 6,3 gam.
C. 15,6 gam và 6,3 gam.
D. 18 gam và 5,3 gam.
Lời giải:
Đáp án: C
Giải thích:
nSO2 = 0,2 mol; nNaOH = 0,25 mol
Xét tỉ lệ: 1< T = nNaOH/nSO2 < 2
=> phản ứng thu được 2 muối NaHSO3 (a mol) và Na2SO3 (b mol)
Bảo toàn nguyên tố Na:
nNaOH = nNaHSO3 + 2.nNa2SO3=> a + 2b = 0,25 (1)
Bảo toàn nguyên tố S:
nSO2 = nNaHSO3 + nNa2SO3 => a + b = 0,2 (2)
Từ (1) và (2) => a = 0,15 mol; b = 0,05 mol
=>mNaHSO3= 0,15.104 = 15,6 gam; nNa2SO3 = 0,05.126 = 6,3 gam
Xem thêm các phương trình liên quan khác:
CO2 + Ca(OH)2 → CaCO3 + H2O | CO2 ra CaCO3 | Ca(OH)2 ra CaCO3
CaCO3 + HCl → CaCl2 + CO2 + H2O | CaCO3 ra CaCl2 | CaCO3 ra CO2
CaCO3 + HNO3 → Ca(NO3)2 + CO2 + H2O | CaCO3 ra CO2