Trắc nghiệm Hóa 11 CD Bài 3. Ph của dung dịch. Chuẩn độ acid – base có đáp án
Trắc nghiệm Hóa 11 CD Bài 3. Ph của dung dịch. Chuẩn độ acid – base có đáp án
-
79 lượt thi
-
30 câu hỏi
-
0 phút
Danh sách câu hỏi
Câu 1:
Dung dịch chất nào sau đây làm xanh quỳ tím?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Dung dịch NaOH có môi trường base, làm quỳ tím ẩm hoá xanh.
Câu 2:
Dung dịch chất nào sau đây làm quỳ tím hóa đỏ?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Dung dịch HCl có môi trường acid, làm quỳ tím chuyển sang màu đỏ.
Câu 3:
Dung dịch chất nào sau đây không làm đổi màu quỳ tím?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Dung dịch Na2SO4 có môi trường trung tính nên không làm đổi màu quỳ tím.
Câu 4:
Dung dịch nào sau đây có pH > 7?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Dung dịch NaOH có môi trường base nên có pH > 7.
Câu 5:
Dung dịch nào sau đây có pH < 7?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Dung dịch HNO3 có môi trường acid nên pH < 7.
Câu 6:
Dung dịch nào sau đây có pH = 7?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Dung dịch NaCl có môi trường trung tính nên có pH = 7.
Câu 7:
Dung dịch chất nào sau đây làm quỳ tím chuyển thành màu xanh?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
CH3COONa chứa gốc acid yếu, thuỷ phân tạo môi trường base, làm quỳ tím chuyển sang màu xanh.
Câu 8:
Trong dung dịch nước, cation kim loại mạnh, gốc acid mạnh không bị thủy phân, còn cation kim loại trung bình và yếu bị thủy phân tạo môi trường acid, gốc acid yếu bị thủy phân tạo môi trường base. Dung dịch muối nào sau đây có pH > 7?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Dung dịch muối Na2CO3 chứa gốc acid yếu, thuỷ phân tạo môi trường base, làm pH > 7.
Câu 9:
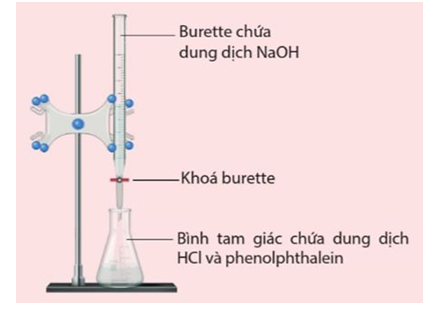
Khi chuẩn độ, người ta thêm từ từ dung dịch đựng trong (1) … vào dung dịch đựng trong bình tam giác. Dụng cụ cần điền vào (1) là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Khi chuẩn độ, người ta thêm từ từ dung dịch đựng trong burette vào dung dịch đựng trong bình tam giác.
Câu 10:
Một dung dịch có pH = 11,7. Nồng độ ion hydrogen (H+) của dung dịch là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Ta có: pH = a thì [H+] = 10-a.
Vậy dung dịch có pH = 11,7 thì [H+] = 10-11,7M = 2.10-12M.
Câu 11:
Calcium hydroxide rắn được hòa tan trong nước cho tới khi pH của dung dịch đạt 10,94. Nồng độ của ion hydroxide (OH−) trong dung dịch là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Ta có: pH = a thì [H+] = 10-a.
Vậy dung dịch có pH = 10,94 thì [H+] = 10-10,94M Þ
Câu 15:
Trộn lẫn V mL dung dịch NaOH 0,01 M với V mL dung dịch HCl 0,03 M được 2V mL dung dịch Y. Dung dịch Y có pH là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Theo bài ra ta thấy, sau phản ứng HCl dư.
Câu 16:
pH của dung dịch nào sau đây có giá trị nhỏ nhất?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Dung dịch NaCl 0,1M có môi trường trung tính, nên pH = 7.
Dung dịch NaOH 0,01M có pH = 14 + log[OH-] = 12.
Dung dịch HCl và CH3COOH có môi trường acid nên có pH < 7.
Lại có hai acid HCl và CH3COOH cùng nồng độ, HCl là acid mạnh hơn CH3COOH nên dung dịch HCl có pH nhỏ nhất.
Câu 17:
Trong các dung dịch acid sau có cùng nồng độ 0,1 M, dung dịch nào có pH cao nhất?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Cả 4 dung dịch acid có cùng nồng độ nhưng chỉ có dung dịch HF là acid yếu nên HF có pH cao nhất trong dãy.
Câu 18:
Trong số các dung dịch có cùng nồng độ 0,1 M dưới đây, dung dịch chất nào có giá trị pH nhỏ nhất?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Loại A và D do các dung dịch NaOH và Ba(OH)2 có môi trường base nên pH > 7.
Trong hai dung dịch HCl và H2SO4 có cùng nồng độ, dung dịch H2SO4 phân li ra nhiều H+ hơn nên có pH nhỏ nhất.
Câu 19:
Các dung dịch NaCl, NaOH, NH3, Ba(OH)2 có cùng nồng độ mol, dung dịch có pH lớn nhất là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Loại D do NaCl có môi trường trung tính.
Loại C do NH3 là base yếu.
Hai dung dịch NaOH và Ba(OH)2 là base mạnh, có cùng nồng độ do đó Ba(OH)2 phân li ra nhiều OH- hơn nên có pH lớn nhất.
Câu 20:
Đo pH của một cốc nước chanh được giá trị pH bằng 2,4. Nhận định nào sau đây không đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Nhận định C không đúng do: nồng độ ion [H+] của nước chanh là 10-2,4 mol/L.
Câu 21:
Tại khu vực bị ô nhiễm, pH của nước mưa đo được là 4,5 còn pH của nước mưa tại khu vực không bị ô nhiễm là 5,7. Nhận xét nào sau đây không đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Nồng độ ion H+ trong dung dịch nước mưa bị ô nhiễm là 10-4,5.
Nồng độ ion H+ trong dung dịch nước mưa không bị ô nhiễm là 10-5,7.
Lại có 10-4,5 > 10-5,7 nên nồng độ ion H+ trong nước mưa bị ô nhiễm cao hơn so với trong nước mưa không bị ô nhiễm.
Câu 22:
Cho các dung dịch: HCl, Na2CO3, AlCl3, Fe(NO3)3, KOH, H3PO4, K3PO4. Số dung dịch làm quỳ tím chuyển sang màu xanh là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
3 dung dịch làm quỳ tím chuyển sang màu xanh là: Na2CO3, KOH, K3PO4.
Câu 23:
Cho các dung dịch: HCl, Na2SO4, AlCl3, Fe(NO3)3, KOH, Na3PO4, HNO3. Số dung dịch làm quỳ tím chuyển sang màu đỏ là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
4 dung dịch làm quỳ tím chuyển sang màu đỏ là: HCl, AlCl3, Fe(NO3)3, HNO3.
Câu 24:
Cho các dung dịch có cùng nồng độ: NaOH (1), H2SO4 (2), HCl (3), KNO3 (4). Giá trị pH của các dung dịch được sắp xếp theo chiều tăng từ trái sang phải là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
pH tăng dần theo thứ tự: môi trường acid < môi trường trung tính < môi trường base.
Vậy (HCl, H2SO4) < KNO3 < NaOH.
Lại có hai acid HCl và H2SO4 có cùng nồng độ nhưng H2SO4 phân li ra H+ nhiều hơn nên có pH nhỏ hơn.
Vậy giá trị pH của các dung dịch được sắp xếp theo chiều tăng từ trái sang phải là:
H2SO4 < HCl < KNO3 < NaOH hay (2), (3), (4), (1).
Câu 25:
Cho ba dung dịch có cùng nồng độ: hydrochloric acid (HCl), ethanol acid (acetic acid, CH3COOH) và sodium hydroxide (NaOH). Khi chuẩn độ riêng một thể tích như nhau của dung dịch HCl và dung dịch CH3COOH bằng dung dịch NaOH, phát biểu nào sau đây là đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Cả hydrochloric acid và ethanoic acid (acetic acid) đều phản ứng với sodium hydroxide theo tỉ lệ 1 : 1 nên khi các thể tích và nồng độ bằng nhau của các acid này được chuẩn độ bằng sodium hydroxide thì cần dùng một thể tích base để đạt đến điểm chuẩn tương đương.
Câu 26:
Cho các phát biểu:
(a) Để so sánh mức độ acid giữa các dung dịch có thể dựa vào nồng độ: dung dịch acid nào có nồng độ lớn hơn sẽ có tính acid mạnh hơn.
(b) Trong các dung dịch có cùng nồng độ, dung dịch nào có tính acid mạnh hơn sẽ có nồng độ ion H+ lớn hơn và pH lớn hơn.
(c) Trong các dung dịch có cùng nồng độ, dung dịch nào có cùng nồng độ ion OH- lớn hơn và pH nhỏ hơn sẽ có tính base lớn hơn.
(d) Trong các dung dịch có cùng nồng độ, dung dịch acid mạnh hơn sẽ có nồng độ ion H+ lớn hơn và pH nhỏ hơn.
(e) Trong các dung dịch có cùng nồng độ, dung dịch có nồng độ ion H+ nhỏ và pH cao sẽ có tính acid yếu hơn.
(g) Trong một dãy các dung dịch có cùng nồng độ được sắp xếp theo tính acid tăng dần thì nồng độ ion OH- sẽ giảm dần và pH giảm dần.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Bao gồm: (a), (e).
(a) Sai vì nồng độ H+ của dung dịch giảm 100 lần.
(e) Sai vì pH = 3 nên dung dịch ban đầu là một acid có [H+] = 0,001 M.
Câu 27:
Khi trộn 1 lít dung dịch Ba(OH)2 0,01M với 200mL dung dịch HCl 0,04M, rồi pha loãng dung dịch thu được 10 lần được dung dịch X. Dung dịch X có giá trị pH là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Vậy sau phản ứng OH- dư: 0,02 – 0,008 = 0,012 mol.
Pha loãng dung dịch 10 lần, nên thể tích dung dịch thu được sau khi pha loãng là:
10.(1 + 0,2) = 12 lít.
Câu 28:
Một học sinh thực hiện thí nghiệm sau: Lấy 10 mL dung dịch HCl 0,2 M cho vào 5 mL dung dịch NH3 thu được dung dịch A. Chuẩn độ lượng HCl dư trong dung dịch A bằng dung dịch NaOH 0,1 M thấy phản ứng hết 10,2 mL. Nồng độ của dung dịch NH3 ban đầu là
Câu 29:
Để xác định hàm lượng CaCO3 trong vỏ trứng, trong phòng thí nghiệm người ta có thể làm như sau: Lấy 1,0 g vỏ trứng khô, đã được làm sạch, hòa tan hoàn toàn trong 50 mL dung dịch HCl 0,4 M. Lọc dung dịch sau phản ứng thu được 50 mL dung dịch A. Lấy 10 mL dung dịch A chuẩn độ với dung dịch NaOH 0,1 M thấy hết 5,6 mL. Hàm lượng cacium trong vỏ trứng là (giả thiết các tạp chất khác trong vỏ trứng không phản ứng với HCl).
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Số mol HCl tác dụng với NaOH là
Số mol HCl có trong 50 mL dung dịch A là:
Số mol HCl phản ứng với CaCO3 là:
Câu 30:
Các dung dịch NaCl, NaOH, NH3, Ba(OH)2 có cùng nồng độ mol, dung dịch có pH lớn nhất là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Loại D do NaCl có môi trường trung tính.
Loại C do NH3 là base yếu.
Hai dung dịch NaOH và Ba(OH)2 là base mạnh, có cùng nồng độ do đó Ba(OH)2 phân li ra nhiều OH- hơn nên có pH lớn nhất.
