Giải bài tập KHTN lớp 8 Bài 6: Tính theo phương trình hoá học
Trả lời:
Để tính theo phương trình hoá học cần tiến hành theo các bước sau:
- Viết phương trình hoá học và xác định tỉ lệ số mol các chất trong phản ứng.
- Xác định số mol chất phản ứng hoặc chất tạo thành theo dữ kiện đề bài.
- Dựa vào phương trình hoá học và lượng chất đã biết tìm số mol chất còn lại.
- Chuyển đổi số mol chất thành khối lượng hoặc thể tích (đối với chất khí ở đkc) theo yêu cầu của đề bài.
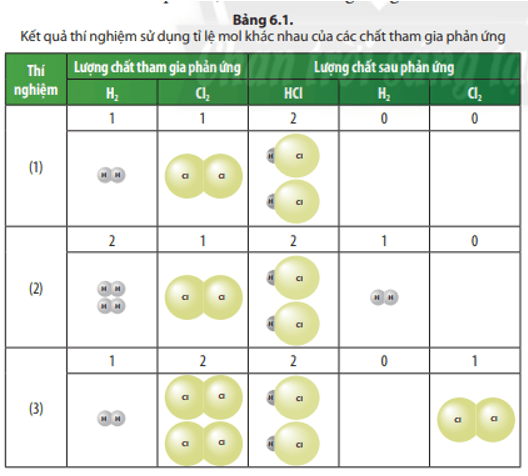
1. Tính theo phương trình hoá học
Trả lời:
Chất sau phản ứng trong thí nghiệm (1) là: HCl;
Chất sau phản ứng trong thí nghiệm (2) là: HCl; H2.
Chất sau phản ứng trong thí nghiệm (3) là: HCl; Cl2.
Trả lời:
Trong thí nghiệm (2): Cl2 thiếu, H2 dư;
Trong thí nghiệm (3): H2 thiếu; Cl2 dư.
Trả lời:
Phản ứng trong thí nghiệm (1) xảy ra vừa đủ.
Trả lời:
Sản phẩm tạo thành trong 3 thí nghiệm là: HCl;
Để xác định lượng sản phẩm tạo thành cần dựa vào lượng chất thiếu.
Trả lời:
Để tính được khối lượng vôi sống sau khi nung ta thực hiện theo các bước sau:
Bước 1: Viết phương trình hoá học và xác định tỉ lệ mol các chất trong phản ứng.
CaCO3 CaO + CO2
1 : 1 : 1
Bước 2: Tìm số mol CaCO3 phản ứng.
Bước 3: Dựa vào phương trình hoá học tìm số mol CaO tạo thành.
Theo phản ứng, tỉ lệ mol giữa các chất bằng nhau nên số mol các chất cũng bằng nhau:
Bước 4: Chuyển đổi số mol chất thành khối lượng:
mCaO = nCaO × MCaO = 0,25 × 56 = 14 (gam).
Trả lời:
Cách tính thể tích khí chlorine:
Bước 1: Viết phương trình hoá học và xác định tỉ lệ các chất trong phản ứng.
2Al + 3Cl2 2AlCl3
2 : 3 : 2
Bước 2: Tìm số mol AlCl3 tạo thành sau phản ứng:
Bước 3: Dựa vào phương trình hoá học tìm số mol khí chlorine tham gia:
Theo tỉ lệ mol của phản ứng, ta có:
Bước 4: Chuyển đổi số mol chất thành thể tích:
Trả lời:
Phương trình hoá học: 4P + 5O2 → 2P2O5
Tỉ lệ các chất: 4 : 5 : 2
Số mol phosphorus đã bị đốt cháy:
Theo tỉ lệ mol của phản ứng, ta có:
2. Hiệu suất phản ứng
Trả lời:
Khối lượng ammonia thực tế bằng ¼ khối lượng ammonia lý thuyết.
Trả lời:
Để tính được hiệu suất phản ứng ta cần biết lượng sản phẩm thực tế và lượng sản phẩm lí thuyết. Trong đó, lượng lí thuyết và lượng thực tế lấy cùng đơn vị đo.
Trả lời:
Phương trình hoá học: H2 + I2 → 2HI
Tỉ lệ các chất: 1 : 1 : 2
Giả sử hiệu suất đạt 100% thì I2 hết, H2 dư, vậy lượng HI thu được theo lí thuyết tính theo I2. Theo tỉ lệ mol của phản ứng, ta có:
nHI lý thuyết =
Hiệu suất của phản ứng là:
Áp dụng:

Trả lời:
Hiệu suất của phản ứng là:
Áp dụng:

Xem thêm lời giải SGK Khoa học tự nhiên lớp 8 Chân trời sáng tạo hay, chi tiết khác:
Bài 4: Định luật bảo toàn khối lượng và phương trình hoá học
Bài 5: Mol và tỉ khối của chất khí