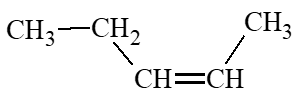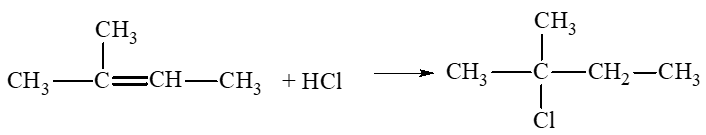Giải Hóa học 11 Bài 13: Hydrocarbon không no
Ethylene là một trong số các hydrocarbon không no. Hydrocarbon không no là gì? Chúng có cấu tạo, tính chất và ứng dụng trong những lĩnh vực nào?
Lời giải:
- Hydrocarbon không no là những hydrocarbon trong phân tử có chứa liên kết đôi C = C hoặc liên kết ba C ≡ C hoặc cả hai loại liên kết đó.
- Tính chất:
+ Tính chất vật lí: ở điều kiện thường các hydrocarbon không no có thể ở thể khí, thể lỏng hoặc thể rắn. Nhiệt độ nóng chảy, nhiệt độ sôi của các hydrocarbon không no nói chung tăng dần theo chiều tăng số nguyên tử carbon trong phân tử. Ngoài ra, các hydrocarbon không no đều nhẹ hơn nước, không tan hoặc ít tan trong nước, tan trong dung môi không phân cực như chloroform …
+ Tính chất hoá học: Phản ứng đặc trưng của các hydrocarbon không no là phản ứng cộng.
- Ứng dụng: Các hydrocarbon không no được ứng dụng làm nguyên liệu trong tổng hợp hữu cơ, nhiên liệu …
1. Khái niệm về alkene và alkyne
Lời giải:
- Giống nhau: đều có mạch hở.
- Khác nhau:
+ Phân tử alkane chỉ chứa các liên kết đơn;
+ Phân tử alkene chỉ chứa liên kết đơn và một liên kết đôi C = C.
+ Phân tử alkyne chỉ chứa liên kết đơn và một liên kết ba C ≡ C.
Lời giải:
Trong các phân tử alkane, alkene và alkyne có cùng số nguyên tử carbon thì số nguyên tử hydrogen giảm dần để đảm bảo hoá trị carbon (luôn là IV).
2. Danh pháp alkene và alkyne
Câu hỏi thảo luận 3 trang 75 Hóa học 11: Viết công thức cấu tạo các alkene và alkyne sau:
a) but – 2 – ene.
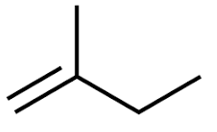
b) 2 – methylpropene.
c) pent – 2 – yne.
Lời giải:
a) but – 2 – ene: CH3 – CH = CH – CH3.
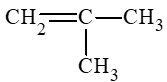
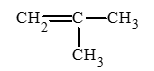
b) 2 – methylpropene:
c) pent – 2 – yne: CH3 – C ≡ C – CH2 – CH3.
Lời giải:
Đánh số các nguyên tử carbon trên mạch chính sao cho số chỉ vị trí liên kết bội mang số nhỏ nhất.
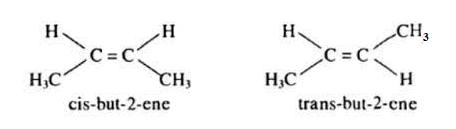
3. Đồng phân hình học
Câu hỏi thảo luận 5 trang 76 Hóa học 11: Vì sao các alkyne không có đồng phân hình học?
Lời giải:
Các alkyne không có đồng phân hình học do trong phân tử alkyne, hai nguyên tử C liên kết ba ở trạng thái lai hoá sp (lai hoá đường thẳng).
Câu hỏi thảo luận 6 trang 76 Hóa học 11: Nêu điều kiện để một alkene có đồng phân hình học.
Lời giải:
Trong phân tử alkene nếu mỗi nguyên tử carbon của liên kết đôi liên kết với hai nguyên tử hoặc hai nhóm nguyên tử khác nhau thì sẽ có đồng phân hình học.
Vậy điều kiện để có đồng phân hình học của alkene 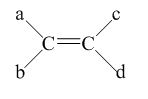
a ≠ b và c ≠ d.
Lời giải:
Đồng phân hình học của pent – 2 – ene:
Đồng phân cis – pent – 2 – ene:
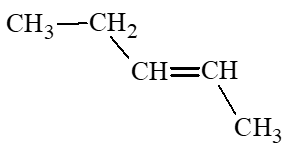
Đồng phân trans – pent – 2 – ene:
4. Tính chất vật lí
Lời giải:
Khi số nguyên tử carbon tăng, tương tác van der Waals giữa các phân tử tăng, dẫn đến nhiệt độ nóng chảy và nhiệt độ sôi của các alkene, alkyne nói chung cũng tăng.
5. Tính chất hóa học
Lời giải:
Khi tham gia phản ứng cộng hydrogen, liên kết π trong phân tử alkene, alkyne bị phá vỡ do liên kết π trong phân tử alkene, alkyne kém bền.
Lời giải:
Đun cồn 90o với sulfuric acid đặc sinh ra khí ethylene (có lẫn tạp chất như CO2, SO2…).
Dẫn khí đi qua ống nghiệm có nhánh đựng dung dịch NaOH để loại bỏ các tạp chất, thu ethylene tinh khiết hơn.
CO2 + 2NaOH → Na2CO3 + H2O;
SO2 + 2NaOH → Na2SO3 + H2O.
Lời giải:
Các phương trình hoá học xảy ra:
- Điều chế ethylene:
C2H5OH →H2SO4,t° CH2 = CH2 + H2O
- Thử tính chất ethylene:
CH2 = CH2 + Br2 → CH2Br – CH2Br
Lời giải:
Phản ứng điều chế C2H2:
CaC2 + 2H2O → Ca(OH)2 + C2H2↑
Lời giải:
Trong cả hai thí nghiệm, nước bromine đều nhạt màu dần đến mất màu.
Lời giải:
Tạo ra sản phẩm phụ: 1,2 – dibromoethane.
Lời giải:
Sản phẩm chính của phản ứng tuân theo quy tắc cộng Markovnikov:
Lời giải:
- Cả hai thí nghiệm dung dịch thuốc tím đều nhạt màu dần đến mất màu.
Phương trình hoá học:
3C2H4 + 2KMnO4 + 4H2O → 3C2H4(OH)2 + 2MnO2↓ + 2KOH
3C2H2 + 8KMnO4 → 3KOOC – COOK + 8MnO2↓ + 2KOH + 2H2O
- Cả hai ống nghiệm đều không thu được dung dịch trong suốt sau thí nghiệm vì đều sinh ra vẩn đục MnO2.
Lời giải:
Phương trình hoá học:
3C3H6 + 2KMnO4 + 4H2O → 3C3H6(OH)2 + 2MnO2↓ + 2KOH
Lời giải:
C2H4 + 3O2 2CO2 + 2H2O
Vậy nếu đốt cháy cùng số mol, C2H4 toả ra nhiều nhiệt lượng hơn.
Lời giải:
Alkyne có 4 nguyên tử carbon trong phân tử có công thức phân tử: C4H6.
Chất này có 2 đồng phân alkyne là:
CH ≡ C – CH2 – CH3 và CH3 – C ≡ C – CH3.
Tuy nhiên chỉ có một chất phản ứng được với dung dịch AgNO3 trong ammonia.
Phương trình hoá học:
CH ≡ C – CH2 – CH3 + Ag(NH3)2OH → CAg ≡ C – CH2 – CH3↓ + 2NH3 + H2O.
Lời giải:
- Trích mẫu thử.
- Dùng dung dịch AgNO3 trong ammonia làm thuốc thử:
+ Không hiện tượng → mẫu thử là but – 2 – yne.
+ Xuất hiện kết tủa vàng → mẫu thử là but – 1 – yne.
Phương trình hoá học:
CH ≡ C – CH2 – CH3 + Ag(NH3)2OH → CAg ≡ C – CH2 – CH3 + 2NH3 + H2O.
6. Ứng dụng và cách điều chế alkene, alkyne
Lời giải:
Vì lượng nhiệt toả ra khi đốt cháy 1 mol acetylene lớn hơn nhiều so với đốt cháy 1 mol ethylene.
Lời giải:
Không được dùng nước dập tắt đám cháy có mặt đất đèn. Do CaC2 (thành phần chính trong đất đèn) có thể tác dụng được với nước sinh ra C2H2 là chất khí, dễ cháy, khi cháy toả nhiệt mạnh càng làm cho đám cháy trở nên dữ dội và nguy hiểm hơn.
Bài tập (trang 84)
Lời giải:
- Các alkene có 4 carbon trong phân tử:
CH2 = CH – CH2 – CH3: but – 1 – ene
CH3 – CH = CH – CH3: but – 2 – ene
Chất có đồng phân hình học là: CH3 – CH = CH – CH3.
Các đồng phân hình học:
- Các alkyne có 4 carbon trong phân tử:
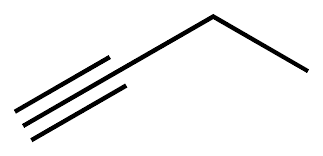
CH ≡ C – CH2 – CH3: but – 1 – yne.
CH3 – C ≡ C – CH3: but – 2 – yne.
Bài 2 trang 84 Hóa học 11: Viết công thức khung phân tử của:
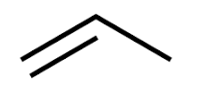
a) propene.
b) 2 – methylbut – 1 - ene.
c) but – 1 – yne.
d) cis – but – 2 – ene.
Lời giải:
|
Chất |
Công thức khung phân tử |
|
a) propene |
|
|
b) 2 – methylbut – 1 – ene |
|
|
c) but – 1 – yne |
|
|
d) cis – but – 2 – ene |
|
Bài 3 trang 84 Hóa học 11: Viết công thức cấu tạo sản phẩm chính của các phản ứng sau:
a) 2 – methylbut – 2 – ene tác dụng với hydrogen chloride.
b) but – 1 – yne tác dụng với nước có xúc tác Hg2+ ở 80 oC.
Lời giải:
a)
b)
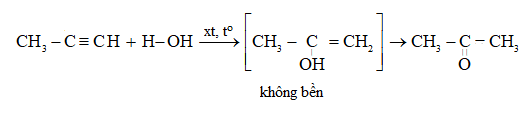
CH ≡ C – CH2 – CH3 + H2O CH3 – CO – CH2 – CH3
Xem thêm các bài giải SGK Hóa lớp 11 Chân trời sáng tạo hay, chi tiết khác: