Giải Hóa học 10 Bài 2: Thành phần của nguyên tử
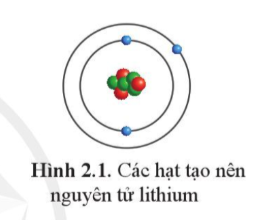
Trả lời:
- Hạt electron màu xanh dương, hạt proton màu đỏ, hạt neutron màu xanh lá cây. Như hình minh họa sau:
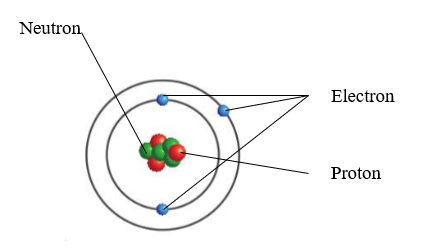 - Vị trí:
- Vị trí:
+ Hạt electron ở vỏ nguyên tử;
+ Hạt proton và neutron ở hạt nhân nguyên tử.
I. Thành phần và cấu trúc của nguyên tử
1. Thành phần nguyên tử

Trả lời:
Giả sử trong một nguyên tử bất kì:
- Có x hạt proton, mỗi hạt proton có điện tích +1.
⇒ Tổng số điện tích dương là +x
- Có y hạt electron, mỗi hạt electron có điện tích -1
⇒ Tổng số điện tích âm là –y.
Nguyên tử trung hòa về điện nên: tổng số điện tích dương + tổng số điện tích âm = 0
⇒ (+x) + (-y) = 0 ⇔ x = y
Vậy trong một nguyên tử bất kì số proton và số electron luôn bằng nhau.
Luyện tập 1 trang 12 Hóa học 10: Hạt proton, neutron nặng hơn hạt electron bao nhiêu lần?
Trả lời:
Khối lượng hạt proton ≈ khối lượng hạt neutron ≈ 1 amu
Khối lượng hạt electron ≈ 0,00055 amu
⇒ Hạt proton, neutron nặng hơn hạt electron là 10,00055 ≈ 1818 lần
Trả lời:
1 amu = 1,6605.10-27 kg = 1,6605.10-24 g
1 hạt proton có khối lượng ≈ 1,6605.10-24 gam
x hạt proton có khối lượng = 1 gam
⇒ x ≈ 11,6605.10−24 = 6,022.1023 hạt
2. Cấu trúc của nguyên tử
A. lớp vỏ với lớp vỏ.
B. lớp vỏ với hạt nhân.
C. hạt nhân với hạt nhân.
Trả lời
Đáp án đúng là: A
Khi các nguyên tử tiến lại gần nhau để hình thành liên kết hóa học, sự tiếp xúc đầu tiên giữa hai nguyên tử sẽ xảy ra giữa lớp vỏ với lớp vỏ.
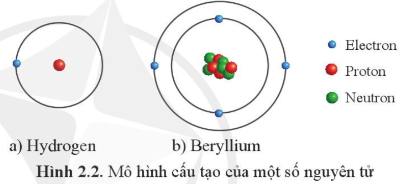
Trả lời:
Nguyên tử beryllium có neutron trong hạt nhân còn nguyên tử hydrogen không có neutron trong hạt nhân.
II. Khối lượng và kích thước của nguyên tử
1. Khối lượng của nguyên tử
Trả lời:
Nguyên tử lithium (Li) tạo nên bởi 3p, 4n và 3e nên khối lượng của một nguyên tử Li là:
3.1 + 4.1 + 3.0,00055 = 7,00165 (amu)
Khối lượng lớp vỏ của Li là: 3.0,00055 = 1,65.10-3 amu.
Phần trăm khối lượng lớp vỏ: 1,65.10−37,00165.100%=0,024%.
2. Kích thước của nguyên tử
Trả lời:
Một nguyên tử Fr có đường kính bằng 7,0oA
Cần số nguyên tử Fr là: 7,8×1047,0 ≈ 11143 nguyên tử
Các loại hạt tạo nên tia âm cực có đặc điểm: (1) Chuyển động theo đường thẳng trong ống (Hình 2.4a). (2) Hoàn toàn giống nhau dù các vật liệu làm cực âm khác nhau. (3) Bị lệch trong điện trường, về phía bản cực tích điện dương được đặt giữa ống tia âm cực (Hình 2.4b).
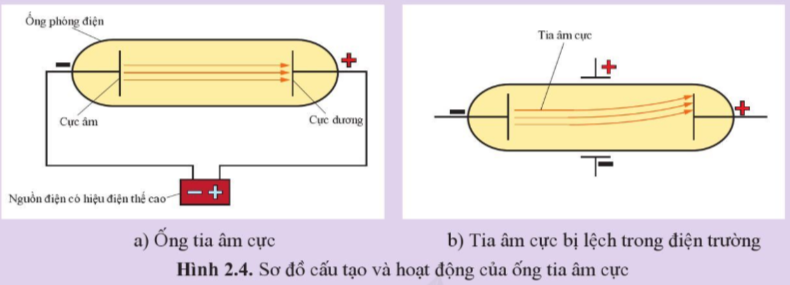
Hãy cho biết hạt tạo nên tia âm cực là loại hạt gì. Giải thích.
Trả lời:
Dựa trên các đặc điểm về tia âm cực xác định được: Hạt tạo nên tia âm cực là hạt electron vì electron mang điện tích âm nên sẽ bị lệch trong điện trường, về phía bản cực tích điện dương.
Bài tập (trang 15)
(a) Đây là nguyên tử nhẹ nhất trong số các nguyên tử được biết cho đến nay.
(b) Khối lượng nguyên tử xấp xỉ 2 amu.
(c) Hạt nhân nguyên tử có khối lượng gấp khoảng 1 818 lần khối lượng lớp vỏ.
(d) Kích thước của nguyên tử bằng kích thước của hạt nhân.
Trả lời:
(a) Đúng. Khối lượng nguyên tử xấp xỉ 1 amu. Là nguyên tử nhẹ nhất trong số các nguyên tử được biết cho đến nay.
(b) Sai. Khối lượng nguyên tử xấp xỉ 1 amu.
(c) Đúng. Khối lượng hạt proton ≈ 1 amu
Khối lượng hạt electron ≈ 0,00055 amu
⇒ Khối lượng hạt nhân nguyên tử lớn hơn khối lượng lớp vỏ là 10,00055 ≈ 1818 lần
(d) Sai. Kích thước của hạt nhân rất nhỏ so với kích thước của nguyên tử.
Trả lời:
Điện tích của 1 hạt electron là -e0 = -1,602 × 10-19C
Điện tích âm của giọt nước trên tương đương với điện tích của số electron là:
−3,33 × 10−17−1,602 × 10−19 ≈ 208 electron
Bài 3 trang 15 Hóa học 10: Nguyên tử trung hòa về điện vì
A. được tạo nên bởi các hạt không mang điện.
B. có tổng số hạt proton bằng tổng số hạt electron.
C. có tổng số hạt electron bằng tổng số hạt neutron.
D. tổng số hạt neutron bằng tổng số hạt proton.
Trả lời:
Nguyên tử trung hòa về điện vì có tổng số hạt proton bằng tổng số hạt electron.
Bài 4 trang 15 Hóa học 10: Trả lời các câu hỏi sau:
a) Loại hạt nào được tìm thấy trong hạt nhân nguyên tử?
b) Loại hạt nào được tìm thấy ở lớp vỏ nguyên tử?
c) Loại hạt nào mang điện trong nguyên tử?
d) Kích thước nguyên tử lớn hơn kích thước hạt nhân nguyên tử khoảng bao nhiêu lần?
Trả lời:
a) Loại hạt được tìm thấy trong hạt nhân nguyên tử là:
+ Hạt proton (kí hiệu là p),
+ Hạt neutron (kí hiệu là n).
b) Loại hạt được tìm thấy ở lớp vỏ nguyên tử là:
+ Hạt electron (kí hiệu là e)
c) Loại hạt mang điện trong nguyên tử là:
+ Hạt proton, mang điện tích dương.
+ Hạt electron, mang điện tích âm.
d) Kích thước nguyên tử lớn hơn kích thước hạt nhân nguyên tử khoảng 104 đến 105 lần.
Trả lời:
Chú ý: Trong nguyên tử số electron = số proton
|
|
Số electron |
Số proton |
Số neutron |
|
H |
1 |
1 |
0 |
|
O |
8 |
8 |
8 |
|
H2O |
1 × 2 + 8 = 10 |
1 × 2 + 8 = 10 |
8 |
Xem thêm lời giải bài tập sgk Hóa học 10 Cánh diều hay, chi tiết khác:
Bài 4: Mô hình nguyên tử và orbital nguyên tử




