Giải Hoá Học 10 Bài 2: Thành phần của nguyên tử
Lời giải:
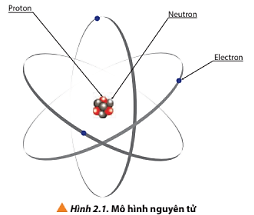
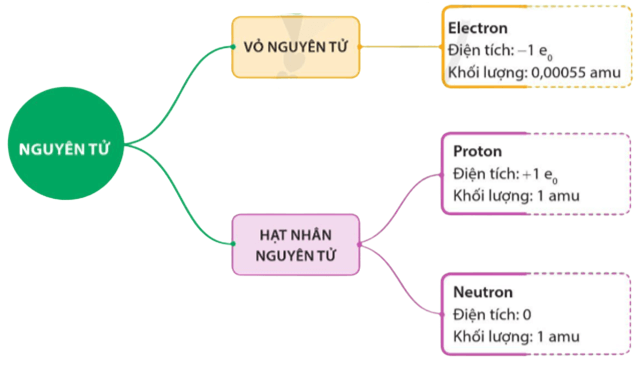
- Nguyên tử gồm các hạt cơ bản: proton, electron và neutron.
+ Hạt electron kí hiệu là e, mang điện tích âm.
+ Hạt proton kí hiệu là p, mang điện tích dương.
+ Hạt neutron kí hiệu là n, không mang điện.
- Cơ sở để phát hiện ra các hạt cơ bản trên là:
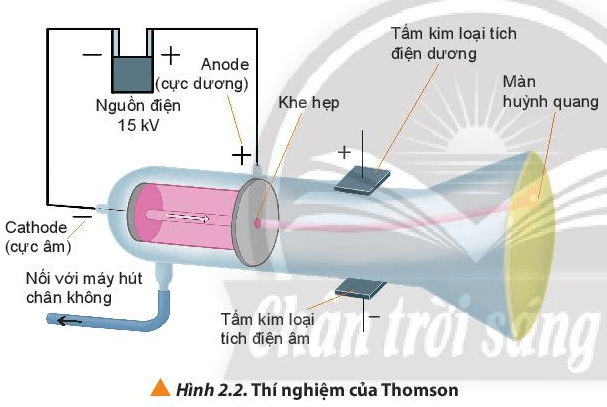
+ Thông qua thí nghiệm khám phá tia âm cực của Thomson đã phát hiện ra hạt electron.
+ Khi bắn phá hạt nhân nguyên tử nitrogen bằng các hạt α, Rutherford đã phát hiện ra hạt proton.
+ Khi dùng các hạt α bắn phá hạt nhân nguyên tử beryllium, J. Chadwick đã phát hiện hạt neutron.
1. Thành phần cấu tạo nguyên tử
Lời giải:
Nguyên tử gồm hạt nhân chứa proton, neutron và vỏ nguyên tử chứa electron.
2. Sự tìm ra electron
Câu hỏi 2 trang 14 Hóa học 10: Cho biết vai trò của màn huỳnh quang trong thí nghiệm ở hình 2.2.
Lời giải:
Màn huỳnh quang dùng để hứng các tia phát ra từ cực âm.
Lời giải:
Tia âm cực mang điện âm nên bị hút về cực dương của trường điện.
Lời giải:
Tia âm cực là chùm hạt vật chất có khối lượng và chuyển động với vận tốc rất lớn.
3. Sự khám phá hạt nhân nguyên tử
Lời giải:
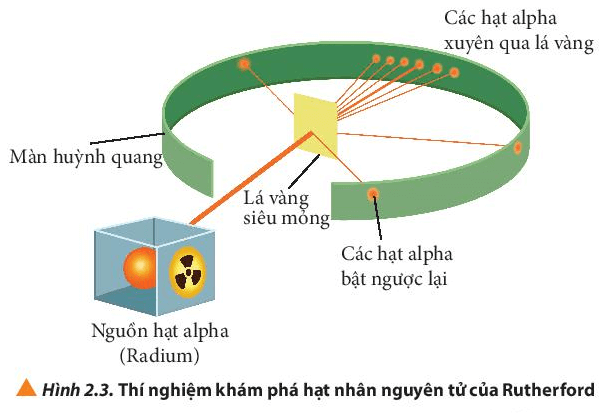
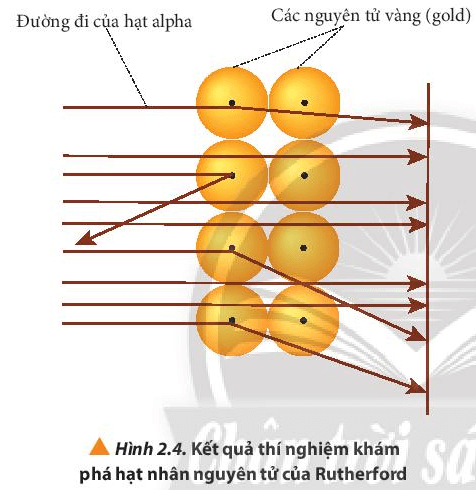
- Các hạt alpha hầu hết đều xuyên thẳng qua lá vàng, một số ít bị lệch hướng và một số rất ít bị bật ngược lại.
Giải thích: Do nguyên tử có cấu tạo rỗng, ở tâm chứa một hạt nhân mang điện tích dương có kích thước rất nhỏ so với kích thước nguyên tử nên hầu hết các hạt alpha có thể đi xuyên qua lá vàng.
Lời giải:
Điện tích của hạt nhân nguyên tử do proton quyết định.
Nguyên tử trung hòa về điện nên số proton = số electron.
⇒ Điện tích hạt nhân của nguyên tử oxygen là +8.
4. Cấu tạo hạt nhân nguyên tử
Lời giải:
Điện tích của hạt nhân nguyên tử do proton quyết định.
Số đơn vị điện tích hạt nhân = số proton.
Lời giải:
Điện tích hạt nhân là +11 nên số proton là 11.
⇒ Số electron = số proton = 11.
Lời giải:
Ta có:
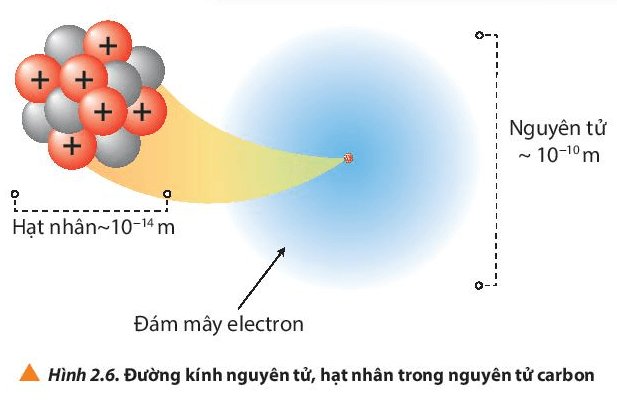
Nhận xét: đường kính nguyên tử lớn hơn đường kính hạt nhân khoảng 10000 lần.
Lời giải:
Ta có:
= 1840 (lần)
Kết quả này cho thấy khối lượng của các hạt electron không đáng kể so với khối lượng của proton và neutron, do đó khối lượng của nguyên tử gần bằng khối lượng của hạt nhân.
Lời giải:
Một cách gần đúng, khối lượng của nguyên tử oxygen là:
mnt = mp + mn = 8 + 8 = 16 amu = 2,656.10-23 gam
Lời giải:
Bài tập (trang 19)
Lời giải:
Dữ kiện: hầu hết các hạt alpha đều xuyên thẳng qua lá vàng.
Do nguyên tử có cấu tạo rỗng, ở tâm chứa một hạt nhân mang điện tích dương có kích thước rất nhỏ so với kích thước nguyên tử nên hầu hết các hạt alpha có thể đi xuyên qua lá vàng.
Bài 2 trang 19 Hóa học 10: Thông tin nào sau đây không đúng?
A. Proton mang điện tích dương, nằm trong hạt nhân, khối lượng gần bằng 1 amu.
B. Electron mang điện tích âm, nằm trong hạt nhân, khối lượng gần bằng 0 amu.
C. Neutron không mang điện, khối lượng gần bằng 1 amu.
Lời giải:
Đáp án đúng là: B
Vì electron mang điện tích âm nằm ở lớp vỏ nguyên tử.
Trong hạt nhân chỉ chứa proton và neutron.
Bài 3 trang 19 Hóa học 10: Mỗi phát biểu dưới đây mô tả loại hạt nào trong nguyên tử?
b) Hạt được tìm thấy trong hạt nhân và không mang điện.
Lời giải:
a) Hạt mang điện tích dương: Hạt proton
b) Hạt được tìm thấy trong hạt nhân và không mang điện: Hạt neutron
c) Hạt mang điện tích âm: Hạt electron
Bài 4 trang 19 Hóa học 10: a) Cho biết 1 g electron có bao nhiêu hạt?
b) Tính khối lượng của 1 mol electron (biết hằng số Avogadro có giá trị là 6,022×1023).
Lời giải:
a) Vì 1 hạt electron nặng 9,11×10-28 g nên 1 g electron có số hạt là:
= 1,098 × 1027 (hạt)
b) 1 mol electron có chứa số hạt là 6,022 × 1023 hạt
Do đó 1 mol electron có khối lượng là:
6,022 × 1023 × 1 × 9,11 × 10-28 = 5,486 × 10-4 (g)
Xem thêm lời giải bài tập SGK Hoá học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 4: Cấu trúc lớp vỏ electron của nguyên tử