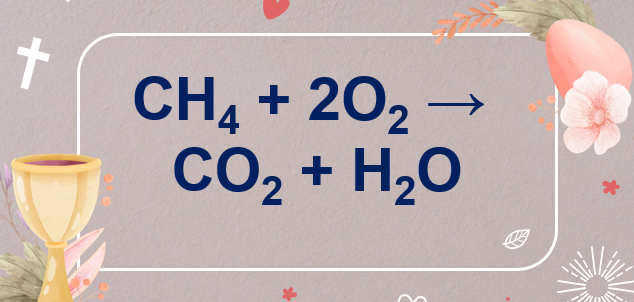Phản ứng CH4 + O2 → CO2 + H2O
1. Phương trình phản ứng CH4 tác dụng với oxi
CH4 + 2O2 →t° CO2 + 2H2O
2. Hiện tượng của phản ứng CH4 tác dụng với oxi
- Phản ứng tạo khí làm đục nước vôi trong.
3. Cách tiến hành phản ứng CH4 tác dụng với oxi
- Đốt khí metan trong khí oxi rồi dẫn sản phẩm thu được vào ống nghiệm chứa dung dịch nước vôi trong.
4. Mở rộng về tính chất hoá học của ankan
- Ở nhiệt độ thường, các ankan không tác dụng với dung dịch axit, dung dịch kiềm và các chất oxi hóa như dung dịch KMnO4 (thuốc tím)...
- Khi chiếu sáng hoặc đun nóng, các ankan dễ dàng tham gia các phản ứng thế, phản ứng tách hiđro và phản ứng cháy.
4.1. Phản ứng thế bởi halogen
- Clo có thể thay thế lần lượt từng nguyên tử H trong phân tử metan.
Phương trình hóa học:
CH4 + Cl2 CH3Cl + HCl
CH3Cl + Cl2 CH2Cl2 + HCl
CH2Cl2 + Cl2 CHCl3 + HCl
CHCl3 + Cl2 CCl4 + HCl
- Các đồng đẳng của metan cũng tham gia phản ứng thế tương tự metan.
Nhận xét:
- Nguyên tử hiđro liên kết với nguyên tử cacbon bậc cao hơn dễ bị thế hơn nguyên tử hiđro liên kết với nguyên tử cacbon bậc thấp hơn.
4.2. Phản ứng tách
- Dưới tác dụng của nhiệt và chất xúc tác thích hợp, các ankan có phân tử khối nhỏ bị tách hiđro thành hiđrocacbon không no tương ứng.
Thí dụ:
CH3 – CH3 CH2 = CH2 + H2
- Ở nhiệt độ cao và chất xúc tác thích hợp, ngoài việc bị tách hiđro, các ankan còn có thể bị phân cắt mạch cacbon tạo thành các phân tử nhỏ hơn.
Thí dụ:
CH3 – CH2 – CH3
4.3. Phản ứng oxi hóa
- Khi bị đốt, các ankan đều cháy, tỏa nhiều nhiệt.
CnH2n + 2 + O2 nCO2 + (n + 1)H2O
5. Bài tập vận dụng liên quan
Câu 1: Thể tích khí oxi cần dùng để đốt cháy hết 4,48 lít khí metan là
A. 6,72 lít
B. 8,96 lít
C. 9,52 lít
D. 10,08 lít
Hướng dẫn giải:
Đáp án B
Số mol CH4 là: = 0,2 mol
Phương trình phản ứng:
Theo phương trình phản ứng ta có = 0,4 mol
Vậy thể tích khí oxi cần dùng là = 0,4.22,4 = 8,96 lít.
Câu 2: Khí metan phản ứng được với chất nào sau đây?
A. CO2
B. HCl
C. CO
D. O2
Hướng dẫn giải:
Đáp án D
Phương trình phản ứng:
Câu 3: Khối lượng CO2 và H2O thu được khi đốt cháy 16 gam khí metan là
A. 44 gam và 36 gam
B. 44 gam và 18 gam
C. 22 gam và 18 gam
D. 22 gam và 36 gam
Hướng dẫn giải:
Đáp án A
Số mol của CH4 là: = 1 mol
Phương trình phản ứng:
Theo phương trình phản ứng ta có:
= 1 mol suy ra = 1.44 = 44 gam
= 2 mol suy ra = 2.18 = 36 gam
Câu 4: Đốt cháy hoàn toàn m gam khí metan thu được 13,44 lít khí CO2 ở đktc. Giá trị của m là
A. 10,2 gam
B. 7,8 gam
C. 8,8 gam
D. 9,6 gam
Hướng dẫn giải:
Đáp án D
Số mol của CO2 là: = 0,6 mol
Phương trình phản ứng:
Theo phương trình phản ứng ta có: = 0,6 mol
Vậy khối lượng của CH4 là: m = 0,6.16 = 9,6 gam.
Câu 5: Trong phòng thí nghiệm, người ta có thể thu khí CH4 bằng cách
A. Đẩy không khí (ngửa bình).
B. Đẩy axit.
C. Đẩy nước (úp bình)
D. Đẩy nước (ngửa bình).
Hướng dẫn giải:
Đáp án C
CH4 không tan trong nước nên cần phải thu bằng phương pháp đẩy nước và đặt úp bình.
Câu 6: Điều kiện để xảy ra phản ứng giữa metan và khí clo là
A. Có ánh sáng
B. Có axit làm xúc tác
C. Có sắt làm xúc tác
D. Làm lạnh.
Hướng dẫn giải:
Đáp án A
Điều kiện để xảy ra phản ứng giữa metan và khí clo là có ánh sáng
Phương trình phản ứng:
Câu 7: Chọn câu đúng trong các câu sau:
A. Metan có nhiều trong khí quyển.
B. Metan có nhiều trong nước biển.
C. Metan có nhiều trong nước ao, hồ.
D. Metan có nhiều trong các mỏ khí, mỏ dầu và mỏ than.
Hướng dẫn giải:
Đáp án D
Metan có nhiều trong các mỏ khí, mỏ dầu và mỏ than.
Câu 8: Thành phần phần trăm về khối lượng của các nguyên tố cacbon và hiđro trong CH4 lần lượt là
A. 40% và 60%
B. 80% và 20%
C. 75% và 25%
D. 50% và 50%
Hướng dẫn giải:
Đáp án C
Ta có: %mC = = 75%
%mH = 100% - 75% = 25%
Câu 9: Khí metan có lẫn khí cacbonic, để thu được khí metan tinh khiết cần
A. Dẫn hỗn hợp qua nước vôi trong dư.
B. Đốt cháy hỗn hợp rồi dẫn qua nước vôi trong.
C. Dẫn hỗn hợp qua bình đựng dung dịch H2SO4.
D. Dẫn hỗn hợp qua bình đựng dung dịch brom dư.
Hướng dẫn giải:
Đáp án A
Khí metan có lẫn khí cacbonic, để thu được khí metan tinh khiết cần dẫn hỗn hợp khí qua nước vôi trong dư.
Khí CO2 phản ứng bị giữ lại, khí metan không phản ứng thoát ra khỏi dung dịch thu được metan tinh khiết.
Phương trình phản ứng: CO2 + Ca(OH)2 → CaCO3↓ + H2O
Câu 10: Tính chất hóa học nào sau đây không phải của metan?
A. Làm mất màu dung dịch nước brom.
B. Tác dụng với oxi tạo thành CO2 và nước.
C. Tham gia phản ứng thế.
D. Tác dụng với clo khi có ánh sáng.
Hướng dẫn giải:
Đáp án A
Metan không làm mất màu dung dịch brom.
Bài 11: Những phát biểu nào sau đây không đúng?
1) Metan tác dụng với clo khi có ánh sáng.
2) Metan là chất khí, không màu, không mùi, nặng hơn không khí.
3) Metan cháy tỏa nhiều nhiệt nên được dùng làm nhiên liệu trong đời sống và trong sản xuất.
4) Hỗn hợp giữa metan và clo là hỗn hợp nổ.
5) Trong phân tử metan có bốn liên kết đơn C-H.
6) Metan tác dụng với clo ở điều kiện thường.
A. 1, 3, 5. B. 1, 2, 6.
C. 2, 4, 6. D. 2, 4, 5
Hướng dẫn giải:
Các phát biểu không đúng: 2, 4, 6
2) Metan là chất khí, không màu, không mùi, nặng hơn không khí => Sai, khí metan nhẹ hơn không khí.
4) Hỗn hợp giữa Metan và Clo là hỗn hợp nổ => Sai.
6) Metan tác dụng với Clo ở điều kiện thường => Sai, phải có chiếu sáng thì phản ứng mới xảy ra
Đáp án: C
Bài 12: Đốt cháy hoàn toàn 11,2 lít khí metan. Biết các thể tích khí đo ở điều kiện tiêu chuẩn.Thể tích khí oxi cần dùng và thể tích khí cacbonic tạo thành lần lượt là
A. 22,4 lít và 22,4 lít.
B. 11,2 lít và 22,4 lít.
C. 22,4 lít và 11,2 lít.
D. 11,2 lít và 22,4 lít.
Hướng dẫn giải:
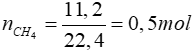
CH4 + 2O2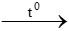 CO2 + 2H2O
CO2 + 2H2O
0,5 → 1 → 0,5 mol
⇒VO2 = 1.22,4 = 22,4 lít
VCO2 = 0,5.22,4 = 11,2 lít
Đáp án: C
Xem thêm các phương trình hóa học liên quan khác:
Al4C3 + H2O → CH4 + Al(OH)3 | Al4C3 ra CH4
Al4C3 ra CH4 l Al4C3 + H2O → CH4 + Al(OH)3 | Nhôm cacbua ra Metan