Điện phân dung dịch chứa x mol CuSO4, y mol H2SO4 và z mol NaCl (với điện cực trơ, màng ngăn xốp, hiệu suất điện phân là 100%, cường độ dòng điện 2,0A). Thời gian điện phân và khối lượng Al2O
51
20/07/2024
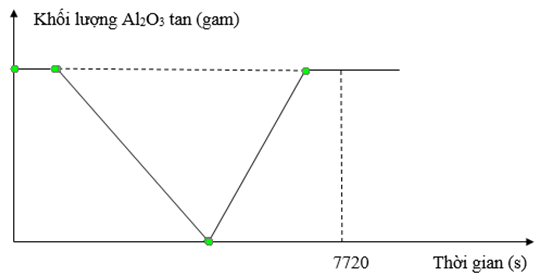
Điện phân dung dịch chứa x mol CuSO4, y mol H2SO4 và z mol NaCl (với điện cực trơ, màng ngăn xốp, hiệu suất điện phân là 100%, cường độ dòng điện 2,0A). Thời gian điện phân và khối lượng Al2O3 bị hoà tan tối đa trong dung dịch sau điện phân ứng với đồ thị sau:
Biết tại thời điểm 7720 (s) khối lượng dung dịch điện phân giảm 5,98 gam và có 0,13 mol khí thoát ra. Giá trị (x + y + z) là
A. 0,160.
B. 0,165.
C. 0,170.
D. 0,155.
Trả lời
Đoạn 1: CuSO4 + 2NaCl → Cu + Cl2 + Na2SO4
Đoạn 2: H2SO4 + 2NaCl → H2 + Cl2 + Na2SO4
Đoạn 3: 2H2O + 2NaCl → H2 + Cl2 + 2NaOH
Đoạn 4: Điện phân nước ở 2 điện cực, tạo H2, O2.
Lúc t = 7720 → ne = 0,16
Catot: nCu = x → nH2 = 0,08 – x
Anot: nCl2 = 0,5z → nO2 = 0,04 – 0,25z
n khí tổng = 0,08 – x + 0,5z + 0,04 – 0,25z = 0,13
m giảm = 64x + 2(0,08 – x) + 35,5z + 32(0,04 – 0,25z) = 5,98
→ x = 0,02; z = 0,12
Lượng Al2O3 bị hòa tan bởi H+ và bởi OH- như nhau nên: nH+ = 6nAl2O3; nOH- = 2nAl2O3 → nH+ = 3nOH-
⇔ 2y = 3.2(0,5z – x – y) (Trong đó: nOH- = 2nCl2 đoạn 3)
→ y = 0,03
→ x + y + z = 0,17
Chọn C