a) So sánh phân tử ammonia và ion ammonium về dạng hình học
589
12/05/2023
Câu hỏi 4 trang 37 Hóa học 11: a) So sánh phân tử ammonia và ion ammonium về dạng hình học, số liên kết cộng hoá trị, số oxi hoá của nguyên tử nitrogen.
b) Viết phương trình hoá học minh hoạ tính acid/base của ammonia và ammonium.
Trả lời
a)
|
Phân tử/ Ion
|
Dạng hình học
|
Số liên kết cộng hoá trị của nitrogen
|
Số oxi hoá của nitrogen
|
|
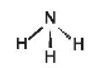
Ammonia (NH3)
|
Chóp tam giác
|
3
|
-3
|
|
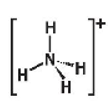
Ammonium (NH4+)
|
Tứ diện
|
4
|
-3
|
b)
- NH3 có tính base. Một số phương trình hoá học minh hoạ:
NH3 + HCl → NH4Cl
2NH3 + H2SO4 → (NH4)2SO4.
- NH4+ có tính acid. Một số phương trình hoá học minh hoạ:
NH4NO3 + NaOH 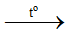 NaNO3 + NH3 + H2O
NaNO3 + NH3 + H2O
NH4Cl + NaOH 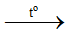 NaCl + NH3 + H2O
NaCl + NH3 + H2O
Phương trình ion rút gọn:
NH4+ + OH− → NH3 + H2O.
Xem thêm lời giải bài tập Hóa học lớp 11 Kết nối tri thức hay, chi tiết khác:
Bài 3: Ôn tập chương 1
Bài 4: Nitrogen
Bài 5: Ammonia. Muối ammonium
Bài 6: Một số hợp chất của nitrogen với oxygen
Bài 7: Sulfur và sulfur dioxide
Bài 8: Sulfuric acid và muối sulfate