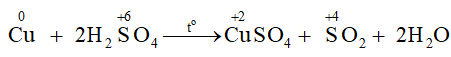Giải Hóa học 11 Bài 8: Sulfuric acid và muối sulfate
Vậy, dung dịch sulfuric acid loãng và dung dịch sulfuric acid đặc có những tính chất quan trọng nào? Cần lưu ý điều gì khi bảo quản và sử dụng acid này để đảm bảo an toàn?
Lời giải:
- Tính chất của sulfuric acid loãng:
Dung dịch sulfuric acid loãng có đầy đủ tính chất của một acid mạnh:
+ Đổi màu quỳ tím thành đỏ.
+ Tác dụng với kim loại hoạt động trong dãy hoạt động hoá học.
+ Tác dụng với basic oxide và base.
+ Tác dụng với nhiều muối.
- Tính chất của sulfuric acid đặc: Ngoài tính acid, dung dịch sulfuric acid đặc còn có tính oxi hoá và tính háo nước.
- Cách bảo quản sulfuric acid:
+ Sulfuric acid được bảo quản trong chai, lọ có nút đậy chặt, đặt ở vị trí chắc chắn.
+ Đặt chai, lọ đựng dung dịch sulfuric acid đặc tránh xa các lọ chứa chất dễ gây cháy, nổ như chlorate, perchlorate, permanganate, dichromate.
- Cách sử dụng sulfuric acid để đảm bảo an toàn:
Sulfuric acid gây bỏng khi rơi vào da, do vậy cần tuân thủ các nguyên tắc:
(1) Sử dụng găng tay, đeo kính bảo hộ, mặc áo thí nghiệm.
(2) Cầm dụng cụ chắc chắn, thao tác cẩn thận.
(3) Không tì, đè chai đựng acid lên miệng cốc, ống đong khi rót acid.
(4) Sử dụng lượng acid vừa phải, lượng acid còn thừa phải thu hồi vào lọ đựng.
(5) Không được đổ nước vào dung dịch acid đặc.
I. Sulfuric acid
b) Dựa vào tương tác giữa các phân tử, hãy dự đoán sulfuric acid là chất lỏng dễ bay hơi hay khó bay hơi.
Lời giải:
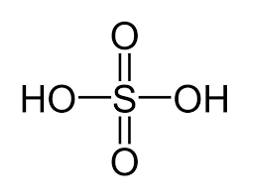
a) Công thức cấu tạo của sulfuric acid:
Như vậy, phân tử sulfuric acid có khả năng cho 2 proton khi đóng vai trò là acid.
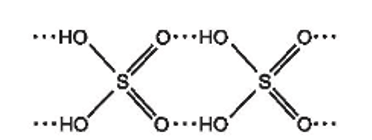
b) Với cấu tạo gồm các nguyên tử hydrogen linh động và các nguyên tử oxygen có độ âm điện lớn, giữa các phân tử sulfuric acid hình thành nhiều liên kết hydrogen:
Dự đoán sulfuric acid là chất lỏng khó bay hơi.
Câu hỏi 2 trang 50 Hóa học 11:
a) Nêu các lưu ý bắt buộc để đảm bảo an toàn khi sử dụng dung dịch sulfuric acid đặc.
b) Hãy cho biết ý nghĩa cảnh báo của kí hiệu cảnh báo ở Hình 8.3.
Lời giải:
a) Các lưu ý bắt buộc để đảm bảo an toàn khi sử dụng dung dịch sulfuric acid đặc:
(1) Sử dụng găng tay, đeo kính bảo hộ, mặc áo thí nghiệm.
(2) Cầm dụng cụ chắc chắn, thao tác cẩn thận.
(3) Không tì, đè chai đựng acid lên miệng cốc, ống đong khi rót acid.
(4) Sử dụng lượng acid vừa phải, lượng acid còn thừa phải thu hồi vào lọ đựng.
(5) Không được đổ nước vào dung dịch acid đặc.
b) Kí hiệu cảnh báo ở Hình 8.3 có ý nghĩa đây là hoá chất ăn mòn.
Hoạt động 1 trang 50 Hóa học 11: Em hãy cho biết các tính chất hoá học cơ bản của một acid.
Lời giải:
Các tính chất hoá học cơ bản của một acid:
+ Đổi màu quỳ tím thành đỏ.
+ Tác dụng với kim loại hoạt động trong dãy hoạt động hoá học.
+ Tác dụng với basic oxide và base.
+ Tác dụng với nhiều muối.
Lời giải:
Các phương trình hoá học minh hoạ:
H2SO4 (loãng) + Fe → FeSO4 + H2
H2SO4 + MgO → MgSO4 + H2O
H2SO4 + Na2CO3 → Na2SO4 + CO2 + H2O
H2SO4 + BaCl2 → BaSO4 + 2HCl.
Thí nghiệm trang 51 Hóa học 11: Đồng (copper) tác dụng với dung dịch sulfuric acid đặc, nóng
Chuẩn bị: đồng lá hoặc phoi bào, dung dịch sulfuric acid 70%; ống nghiệm, kẹp gỗ, đèn cồn, bông tẩm dung dịch NaOH loãng.
Tiến hành:
- Cho vài lá đồng đã cắt nhỏ vào ống nghiệm, thêm tiếp khoảng 3 mL dung dịch H2SO4 70%, dùng bông đã tẩm dung dịch NaOH loãng nút miệng ống nghiệm.
- Hơ nóng đều phần ống nghiệm chứa dung dịch trên ngọn lửa đèn cồn, sau đó đun tập trung vào đáy ống nghiệm.
Lưu ý: Dung dịch sulfuric acid đặc rơi vào da sẽ gây bỏng nặng, cần cẩn thận khi sử dụng.
Quan sát, mô tả hiện tượng xảy ra và thực hiện yêu cầu sau:
1. Viết phương trình hoá học của phản ứng và xác định chất oxi hoá, chất khử.
2. Nhận xét về khả năng phản ứng của dung dịch sulfuric acid đặc, nóng với copper.
Lời giải:
1) Phương trình hoá học:
Chất khử là: Cu; chất oxi hoá là: H2SO4.
2) Dung dịch sulfuric acid đặc, nóng có tính oxi hoá mạnh, có thể oxi hoá kim loại kém hoạt động như copper…
Thí nghiệm trang 51 Hóa học 11: Dung dịch sulfuric acid đặc tác dụng với đường mía
Chuẩn bị: đường mía (C12H22O11), dung dịch sulfuric acid đặc; cốc thuỷ tinh loại 100 mL.
Tiến hành:
– Lấy khoảng 10 g đường mía cho vào cốc.
– Nhỏ đều trên bề mặt đường mía khoảng 2 mL dung dịch sulfuric acid đặc.
Lưu ý: Dung dịch sulfuric acid đặc rơi vào da sẽ gây bỏng nặng, cần cẩn thận khi sử dụng.
Quan sát, mô tả hiện tượng xảy ra và thực hiện yêu cầu sau:
1. Viết phương trình hoá học của các phản ứng xảy ra trong thí nghiệm.
2. Dự đoán hiện tượng khi cho dung dịch sulfuric acid đặc tiếp xúc với các carbohydrate khác như cellulose (giấy, bông), tinh bột (gạo).
Lời giải:
Hiện tượng: Đường mía dần dần hoá than, có hiện tượng sủi bọt đẩy C trào ra ngoài cốc.
1) Phương trình hoá học của phản ứng xảy ra:
C12H22O11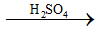
C + 2H2SO4 (đặc) → CO2 + 2SO2 + 2H2O.
2) Dự đoán: Dung dịch sulfuric acid đặc có khả năng lấy nước từ các hợp chất carbohydrate như cellulose (giấy, bông), tinh bột (gạo) và khiến chúng hoá đen (hiện tượng than hoá).
b) Chỉ ra vai trò của sulfuric acid trong mỗi phản ứng đó.
Lời giải:
a) Phương trình hoá học của phản ứng:
NaCl + H2SO4 (đặc) 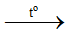
2NaBr + 3H2SO4 → 2NaHSO4 + Br2 + SO2 + 2H2O (2)
b) Phản ứng (1) không có sự thay đổi số oxi hoá của các nguyên tố, H2SO4 đặc đóng vai trò là acid.
Phản ứng (2) số oxi hoá của sulfur giảm từ +6 xuống +4, sulfuric acid đóng vai trò là chất oxi hoá.
Lời giải:
Mỗi năm cả thế giới cần đến hàng trăm triệu tấn sulfuric acid. Trong đó, gần 50% lượng acid được dùng để sản xuất phân bón như ammonium sulfate, calcium dihydrogenphosphate (Ca(H2PO4)2), … Acid này còn được sử dụng trong sản xuất chất tẩy rửa, sơn, phẩm màu, thuốc trừ sâu, giấy, chế hoá dầu mỏ,…
Sulfuric acid là một hoá chất công nghiệp rất quan trọng, sản lượng sulfuric acid của mỗi quốc gia là một chỉ số tốt về sức mạnh công nghiệp của quốc gia đó vì thế sulfuric acid là hoá chất có tầm quan trọng bậc nhất.
Lời giải:
Phương trình hoá học:
Ca3(PO4)2 + 2H2SO4 (đặc) → Ca(H2PO4)2 + 2CaSO4.
Ca3(PO4)2 + 3H2SO4 (đặc) → 2H3PO4 + 3CaSO4.
II. Muối sulfate
Thí nghiệm trang 53 Hóa học 11: Nhận biết ion SO42- bằng ion Ba2+
Chuẩn bị: dung dịch Na2SO4, dung dịch BaCl2; ống nghiệm, kẹp gỗ.
Tiến hành:
- Lấy khoảng 1 mL dung dịch Na2SO4 cho vào ống nghiệm.
- Nhỏ vài giọt dung dịch BaCl2 vào ống nghiệm, lắc nhẹ.
Quan sát hiện tượng xảy ra và thực hiện các yêu cầu:
1. Viết phương trình hoá học dạng phân tử và ion rút gọn.
2. Dự đoán hiện tượng khi nhỏ dung dịch BaCl2 vào ống nghiệm đựng dung dịch H2SO4 loãng.
Lời giải:
Hiện tượng: Xuất hiện kết tủa trắng.
1) Phương trình hoá học dạng phân tử:
Na2SO4 + BaCl2 → BaSO4 + 2NaCl
Phương trình hoá học dạng ion thu gọn:
2) Dự đoán hiện tượng khi nhỏ dung dịch BaCl2 vào ống nghiệm đựng dung dịch H2SO4 loãng là xuất hiện kết tủa trắng barium sulfate theo phương trình hoá học:
H2SO4 + BaCl2 → BaSO4 + 2HCl.
Lời giải:
Các muối sulfate có nhiều ứng dụng trong đời sống:
+ Ammonium sulfate ((NH4)2SO4) ở dạng tinh thể màu trắng, chủ yếu được dùng làm phân bón, cung cấp đạm cho đất.
+ Magnesium sulfate (MgSO4) ở dạng tinh thể màu trắng, chủ yếu được sử dụng làm phân bón. Muối này còn được dùng làm thuốc để cung cấp magnesium cho cơ thể, giúp giảm các cơn đau cơ, giảm hiện tượng chuột rút…
+ Thạch cao nung (CaSO4. 0,5 H2O) khi nhào trộn với nước có khả năng đông cứng rất nhanh, nhờ tính chất này thạch cao nung được sử dụng làm vật liệu xây dựng, nặn đúc tượng và khuôn đúc, bó chỉnh hình trong y học. Ngoài ra, thạch cao nung còn được dùng làm chất phụ gia trong chế biến thực phẩm với hàm lượng cho phép nhất định. Chất này giúp đông tụ protein trong đậu phụ, phô mai; hạn chế hiện tượng nhão của bột làm bánh; giữ nước bên trong các loại mứt…
+ Barium sulfate (BaSO4) ở dạng tinh thể màu trắng, được sử dụng rộng rãi trong các lĩnh vực như sơn, mực in, nhựa, lớp phủ, men, thuỷ tinh, khai thác khoáng sản, sản xuất các loại giấy trắng chất lượng cao. Trong y tế, barium sulfate là thành phần chính của thuốc cản quang trong kĩ thuật X – quang.
Câu hỏi 4 trang 54 Hóa học 11: : Trình bày phương pháp hoá học để phân biệt các cặp dung dịch sau:
a) BaCl2 và NaCl;
b) H2SO4 loãng và HCl.
Lời giải:
a) Phân biệt cặp dung dịch BaCl2 và NaCl bằng dung dịch chứa ion sulfate như H2SO4; Na2SO4 …. Hiện tượng:
+ Xuất hiện kết tủa trắng → BaCl2. Phương trình ion thu gọn:
+ Không có hiện tượng xuất hiện → NaCl.
b) Phân biệt cặp dung dịch H2SO4 loãng và HCl bằng dung dịch chứa ion Ba2+ như BaCl2; Ba(NO3)2 …. Hiện tượng:
+ Xuất hiện kết tủa trắng → H2SO4. Phương trình ion thu gọn:
+ Không có hiện tượng xuất hiện → HCl.
Lời giải:
- Cách bảo quản sulfuric acid:
+ Sulfuric acid được bảo quản trong chai, lọ có nút đậy chặt, đặt ở vị trí chắc chắn.
+ Đặt chai, lọ đựng dung dịch sulfuric acid đặc tránh xa các lọ chứa chất dễ gây cháy, nổ như chlorate, perchlorate, permanganate, dichromate.
- Cách sử dụng sulfuric acid để đảm bảo an toàn:
Sulfuric acid gây bỏng khi rơi vào da, do vậy cần tuân thủ các nguyên tắc:
(1) Sử dụng găng tay, đeo kính bảo hộ, mặc áo thí nghiệm.
(2) Cầm dụng cụ chắc chắn, thao tác cẩn thận.
(3) Không tì, đè chai đựng acid lên miệng cốc, ống đong khi rót acid.
(4) Sử dụng lượng acid vừa phải, lượng acid còn thừa phải thu hồi vào lọ đựng.
(5) Không được đổ nước vào dung dịch acid đặc.
- Cách sơ cứu khi bị bỏng acid:
Khi bị bỏng sulfuric acid cần thực hiện sơ cứu theo các bước sau:
(1) Nhanh chóng rửa ngay với nước lạnh nhiều lần để làm giảm lượng acid bám trên da. Nếu bị bỏng ở vùng mặt nhưng acid chưa bắn vào mắt thì nhắm chặt mắt khi ngâm rửa. Nếu acid đã bắn vào mắt thì úp mặt vào chậu nước sạch, mở mắt và chớp nhiều lần để rửa acid.
(2) Sau khi ngâm rửa bằng nước, cần tiến hành trung hoà acid bằng dung dịch NaHCO3 loãng (khoảng 2%).
(3) Băng bó tạm thời vết bỏng bằng băng sạch, cho người bị bỏng uống bù nước điện giải rồi đưa đến cơ sở y tế gần nhất.
Xem thêm các bài giải SGK Hoá học 11 Kết nối tri thức hay, chi tiết khác:
Bài 6: Một số hợp chất của nitrogen với oxygen
Bài 7: Sulfur và sulfur dioxide