Bảng tuần hoàn các nguyên tố hóa học
I. Sơ lược về bảng tuần hoàn các nguyên tố hóa học
1. Bảng tuần hoàn các nguyên tố hóa học là gì?
Bảng tuần hoàn hóa học hay còn được gọi là bảng tuần hoàn Mendeleev, là phương pháp dạng bảng hiển thị lên các nguyên tố hóa học phát minh vào năm 1869 do nhà hóa học Dimitri Mendeleev người Nga.
2. Cấu tạo bảng tuần hoàn các nguyên tố hoá học
a) Ô nguyên tố
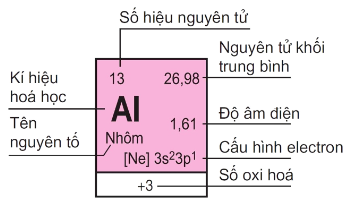
- Ô nguyên tố cung cấp thông tin gồm: ký hiệu hoá học, tên nguyên tố, số hiệu nguyên tử, nguyên tử khối của nguyên tố đó.
- Trong đó, số hiệu nguyên tử có số trị bằng số đơn vị điện tích hạt nhân và bằng số E trong nguyên tử. Số hiệu nguyên tử đồng thời chính là số thứ tự của nguyên tố đó trong bảng tuần hoàn.
Ví dụ: Số hiệu nguyên tử của Al là 13 cho biết: Al ở ô số 13, điện tích hạt nhân nguyên tử là 13+, có 13 electron trong nguyên tử Nhôm
b) Chu kỳ
- Chu kỳ là một dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron và được xếp theo thứ tự điện tích hạt nhân tăng dần. Thông thường, chu kỳ có số thứ tự bằng số lớp electron.
- Bảng tuần hoàn hoá học gồm 7 chu kỳ, trong đó, các chu kỳ nhỏ là chu kỳ số 1,2,3, còn lại là các chu kỳ lớn.
Chu kỳ 1: Có 2 nguyên tố gồm H và He
Chu kỳ 2: Gồm 8 nguyên tố Li, Be, B, C, N, O, F, Ne
Chu kỳ 3: Gồm 8 nguyên tố Na, Mg, Al, Si, P, S, Cl, Ar
Chu kỳ 4 và chu kỳ 5: Mỗi chu kỳ có 18 nguyên tố, bắt đầu là một kim loại kiềm và kết thúc là một khí hiếm
Chu kỳ 6: Có 32 nguyên tố, từ Cs đến Rn
Chu kỳ 7: Chưa hoàn thiện
c) Nhóm nguyên tố
- Nhóm nguyên tố gồm các nguyên tố mà trong đó nguyên tử của chúng có cùng số electron lớp ngoài cùng.
- Chúng có tính chất tương tự nhau và được xếp lần lượt theo chiều tăng của điện tích hạt nhân.
- Số thứ tự của nhóm nguyên tố được tính bằng số electron lớp ngoài cùng của nguyên tử.
Có 2 loại nhóm nguyên tố là nhóm A và nhóm B. Trong đó:
Nhóm A: Gồm các nguyên số s và p
Nhóm B: Gồm các nguyên tố d và f
* Có bao nhiêu nguyên tố trong bảng tuần hoàn
Tính đến thời điểm hiện tại, tổng cộng có 118 nguyên tố trong bảng tuần hoàn được xác thực, bao gồm từ nguyên tố 1 (Hydro) tới 118 (Oganesson).
Trong tổng cộng 118 nguyên tố của thì có đến 98 nguyên tố xuất hiện trong tự nhiên, 20 nguyên tố còn lại từ Einsteini đến Oganesson thường chỉ xuất hiện ở các phép tổng hợp nhân tạo. Trong số 98 nguyên tố xuất hiện trong tự nhiên thì có 84 nguyên tố nguyên thuỷ – tức là chúng đã được xuất hiện trước khi Trái đất được hình thành. 14 nguyên tố còn lại chỉ xuất hiện trong các chuỗi phân rã của các nguyên tố nguyên thuỷ đó. Ở dạng tinh khiết, không nguyên tố nào nặng hơn Einstein (99).
3. Bảng tuần hoàn các nguyên tố hóa học được sắp xếp theo nguyên tắc nào
- Nguyên tắc 1: Các nguyên tố hóa học.i.được sắp xếp theo chiều tăng dần.i.của điện tích hạt nhân
- Nguyên tắc 2: Các nguyên tố có cùng số lớp.i.electron trong nguyên tử được xếp vào cùng một hàng ngang (hay còn gọi là chu kì)
- Nguyên tắc 3: Các nguyên tố hóa học có cùng số electron hóa trị được xếp vào thành một cột (hay còn gọi là nhóm)
Chú ý: Electron hóa trị là những electron có khả năng tham gia hình thành liên kết hóa học hay còn gọi là electron lớp ngoài cùng.
II. Bảng tuần hoàn các nguyên tố hóa học
1. Bảng một số nguyên tố hóa học hay gặp
Bảng nguyên tố hóa học
| Số hiệu nguyên tử (Z) | Tên cũ | Tên nguyên tố hóa học (IUPAC) | Kí hiệu hoá học | Khối lượng nguyên tố (amu) | Hoá trị |
| 1 | Hiđro | Hydrogen | H | 1 | I |
| 2 | Heli | Helium | He | 4 | |
| 3 | Liti | Lithium | Li | 7 | I |
| 4 | Beri | Beryllium | Be | 9 | II |
| 5 | Bo | Boron | Bo | 11 | III |
| 6 | Cacbon | Carbon | C | 12 | IV, II |
| 7 | Nitơ | Nitrogen | N | 14 | II, III, IV… |
| 8 | Oxi | Oxygen | O | 16 | II |
| 9 | Flo | Flourine | F | 19 | I |
| 10 | Neon | Neon | Ne | 20 | |
| 11 | Natri | Sodium | Na | 23 | I |
| 12 | Magie | Magnesium | Mg | 24 | II |
| 13 | Nhôm | Aluminium | Al | 27 | III |
| 14 | Silic | Silicon | Si | 28 | IV |
| 15 | Photpho | Phosphorus | P | 31 | III, V |
| 16 | Lưu huỳnh | Sulfur | S | 32 | II, IV, VI |
| 17 | Clo | Chlorine | Cl | 35,5 | I,… |
| 18 | Agon | Argon | Ar | 39,9 | |
| 19 | Kali | Potassium | K | 39 | I |
| 20 | Canxi | Calcium | Ca | 40 | II |
Tên gọi, kí hiệu Hóa học và khối lượng nguyên tử của 20 nguyên tố đầu
Chú thích:
- Nguyên tố phi kim: chữ màu xanh
- Nguyên tố kim loại: chữ màu đen
- Nguyên tố khí hiếm: chữ màu đỏ
2. Bảng tuần hoàn các nguyên tố Hóa học lớp 7

III. Cách xem bảng tuần hoàn các nguyên tố hóa học
1. Tên nguyên tố
Tên nguyên tố đại diện cho chất hoá học đó ở dạng tinh khiết, bao gồm một kiểu nguyên tử, được phân biệt bởi số hiệu nguyên tử
2. Ký hiệu hoá học
Ký hiệu hoá học là tên viết tắt của nguyên tố hoá học đó, thường bao gồm từ 1 đến 2 chữ cái trong bảng chữ cái Latinh, trong đó chữ đầu tiên viết hoa.
3. Số nguyên tử
Số nguyên tử hay còn được gọi là số proton của một nguyên tố hoá học. Số proton này được tìm thấy trong hạt nhân của nguyên tử đó, giúp xác định nguyên tố hoá học đó. Số nguyên tử bằng số E trong một nguyên tử trung hòa về điện.
4. Nguyên tử khối trung bình
Đa phần các nguyên tố hoá học đều là hỗn hợp của nhiều đồng vị với tỷ lệ phần trăm số nguyên tử xác định khác nhau. Vì vậy nên nguyên tử khối của các nguyên tố có nhiều đồng vị thường là trung bình khối của các đồng vị có tính đến tỷ lệ phần trăm số nguyên tử tương ứng.
5. Độ âm điện
Độ âm điện là khả năng hút electron của một nguyên tử trong các liên kết hoá học. Độ âm điện của nguyên tử nguyên tố càng nhỏ thì tính phi kim càng yếu và ngược lại.
6. Cấu hình electron
Cấu hình electron của nguyên tử cho biết sự phân bố các electron trong nguyên tử đó ở các trạng thái năng lượng khác nhau ở ở vùng hiện diện của chúng.
7. Số oxi hoá
Số oxi hoá là số của một nguyên tử hoặc một nhóm nguyên tử, cho biết số electron trao đổi khi một chất bị khử hoặc bị oxi hoá trong một phân tử.
IV. Các mẹo ghi nhớ bảng tuần hoàn các nguyên tố hóa học dễ nhất
- Sau đây là 3 cách giúp các bạn học sinh ghi nhớ tốt bảng tuần hoàn hóa học 10.
a) Nghiên cứu bảng tuần hoàn hóa học 10
- Xác định bản chất các thành phần khác nhau của mỗi nguyên tố hóc học. Trong bảng tuần hoàn hóa học 10, mỗi một ô sẽ gồm nguyên tố gồm các thuộc tính, thành phần của nguyên tố đó. Vì thế, để tìm hiểu bảng tuần hoàn, bạn cần biết tên nguyên tố cùng ký hiệu hóa học, số nguyên tử… Tất cả các thông tin này đều có trong ô nguyên tố đó.
- Ghi nhớ và thành thạo 10 nguyên tố đầu tiên trong bảng, bạn sẽ tìm ra quy luật cho các giá trị nguyên tố tiếp theo. Sau đó, bạn sử dụng phương pháp so sánh với giá trị đã học. Cứ như vậy, bạn sẽ học hết hơn 120 nguyên tố trong bảng tuần hoàn Mendeleev.
b) In bảng tuần hoàn hóa học 10 ra một bản màu dán để trong cặp
- Bạn có thể in hoặc mua một bảng tuần hoàn, bạn sẽ mang đi mọi nơi và học bất cứ khi nào thuận tiện.
- Hãy in thật nhiều bản và dán những nơi cần thiết trong không gian học.
- Hãy ghim một tờ note trên bản dán nhiều lúc bạn phải ghi nhớ. Hoặc có thể chụp lại bản chính và để ở nơi bạn dễ quan sát.
- Thường xuyên mở ra xem để nhớ được lâu hơn. Có thể chia thành các phần nhỏ để học thay vì nhồi nhét quá nhiều nguyên tố.
c) Dùng phương pháp ghi nhớ bảng tuần hoàn hóa học 10
- Dùng phương pháp ghi nhớ là viết một vài cụm từ, một vài câu giúp bạn nhớ nhanh hơn trong các nguyên tố hóa học. Phương pháp nhớ nhanh và dài nhất là thường xuyên làm bài tập hóa học và tra bảng tuần hoàn hóa học.
Cách nhớ dãy kim loại dễ dàng nhất:
K Na Ca Mg Al Zn Fe Ni Sn Pb H Cu Hg Ag Pt Au – Khi nào cần may áo giáp sắt nhớ sang phố hỏi cửa hàng áo phi âu.
Cách học thuộc nguyên tử khối nhanh nhất
Bài ca nguyên tử khối mẫu 1
Hai ba Natri (Na=23)
Nhớ ghi cho rõ
Kali chẳng khó
Ba chín dễ dàng (K=39)
Khi nhắc đến Vàng
Một trăm chín bảy (Au=197)
Oxi gây cháy
Chỉ mười sáu thôi (O=16)
Còn Bạc dễ rồi
Một trăm lẻ tám (Ag =108)
Sắt màu trắng xám
Năm sáu có gì (Fe=56)
Nghĩ tới Beri
Nhớ ngay là chín (Be=9)
Gấp ba lần chín
Là của anh Nhôm (Al=27)
Còn của Crôm
Là năm hai đó (Cr=52)
Của Đồng đã rõ
Là sáu mươi tư (Cu =64)
Photpho không dư
Là ba mươi mốt (P=31)
Hai trăm lẻ một
Là của Thủy Ngân (Hg=201)
Chẳng phải ngại ngần
Nitơ mười bốn (N=14)
Hai lần mười bốn
Silic phi kim (Si=28)
Can xi dễ tìm
Bốn mươi vừa chẵn (Ca=40)
Mangan vừa vặn
Con số năm lăm (Mn=55)
Ba lăm phẩy năm
Clo chất khí (Cl=35.5)
Phải nhớ cho kỹ
Kẽm là sáu lăm (Zn=65)
Lưu huỳnh chơi khăm
Ba hai đã rõ (S=32)
Chẳng có gì khó
Cacbon mười hai (C=12)
Bari hơi dài
Một trăm ba bảy (Ba=137)
Phát nổ khi cháy
Cẩn thận vẫn hơn
Khối lượng giản đơn
Hiđrô là một (H=1)
Còn cậu Iốt
Ai hỏi nói ngay
Một trăm hai bảy (I=127)
Nếu hai lẻ bảy
Lại của anh Chì (Pb =207)
Brôm nhớ ghi
Tám mươi đã tỏ (Br = 80)
Nhưng vẫn còn đó
Magiê hai tư (Mg=24)
Chẳng phải chần trừ
Flo mười chín (F=19).
Bài ca nguyên tử khối mẫu 2
Hiđro số 1 khởi đi
Liti số 7 ngại gì chí trai
Cacbon bến nước 12
Nitơ 14 tuổi ngày hoa niên
Oxi 16 khuôn viên
Flo 19 lòng riêng vương sầu
Natri 23 xuân đầu
Magie 24 mong cầu mai sau
Nhôm thời 27 chí cao
Silic 28 lòng nào lại quên
Photpho 31 lập nên
32 nguyên tử khối tên Lưu huỳnh
Clo 35,5 tự mình
Kali 39 nhục vinh chẳng màn
Canxi 40 thẳng hàng
52 Crom chuỗi ngày tàn phải lo
Mangan song ngũ(55) so đo
Sắt thời 56 đừng cho trồng trềnh
Coban 59 cồng kềnh
Kẽm đồng 60 lập nền có dư
Đồng 63,6
Kẽm 65,4
Brom 80 chín thư riêng phần
Stronti 88 đồng cân
Bạc 108 tăng lần số sai
Catmi một bách mười hai(112)
Thiếc trăm mười chín(119) một mai cuộc đời
Iot 127 chẳng dời
Bari 137 sức thời bao lâm
Bạch kim 195
Vàng 197 tiếng tăng chẳng vừa
Thủy ngân 2 bách phẩy 0 thừa(200,0)
Chì 2 linh 7(207) chẳng ưa lửa hồng
Rađi 226 mong
Bismut 2 trăm linh 9 cứ trông cậy mình(209)
Bài thơ nguyên tử phân minh
Lòng này đã quyết tự tin học hàn
Bài ca nguyên tử khối mẫu 3
Hidro là 1
12 cột Các bon
Nito 14 tròn
Oxi trăng 16
Natri hay láu táu
Nhảy tót lên 23
Khiến Magie gần nhà
Ngậm ngùi nhận 24
27 Nhôm la lớn
Lưu huỳnh giành 32
Khác người thật là tài
Clo ba nhăm rưỡi(35,5)
Kali thích 39
Canxi tiếp 40
Năm nhăm Mangan cười
Sắt đây rùi:56
64 đồng nổi cáu
Bởi kém kẽm (Zn) 65
80 Brom nằm
Xa Bạc (Ag) 108
Bải buồn chán ngán
(137) Một ba bẩy ích chi
kém người ta còn gì!
Thủy ngân (Hg) hai linh mốt(201)
Cách học thuộc bài ca hóa trị nhanh nhất
Hidro (H) cùng với liti (Li)
Natri (Na) cùng với kali (K) chẳng rời
Ngoài ra còn bạc (Ag) sáng ngời
Chỉ mang hoá trị I thôi chớ nhầm
Riêng đồng (Cu) cùng với thuỷ ngân (Hg)
Thường II ít I chớ phân vân gì
Đổi thay II, IV là chì (Pb)
Điển hình hoá trị của chì là II
Bao giờ cùng hoá trị II
Là ôxi (O) , kẽm(Zn) chẳng sai chút gì
Ngoài ra còn có canxi (Ca)
Magiê (Mg) cùng với bari (Ba) một nhà
Bo (B) , nhôm (Al) thì hóa trị III
Cácbon (C) silic (Si) thiếc (Sn) là IV thôi
Thế nhưng phải nói thêm lời
Hóa trị II vẫn là nơi đi về
Sắt (Fe) II toan tính bộn bề
Không bền nên dễ biến liền sắt III
Photpho III ít gặp mà
Photpho V chính người ta gặp nhiều
Nitơ (N) hoá trị bao nhiêu ?
I, II, III, IV phần nhiều tới V
Lưu huynh lắm lúc chơi khăm
Khi II lúc IV, VI tăng tột cùng
Clo Iot lung tung
II, III, V, VII thường thì I thôi
Mangan rắc rối nhất đời
Đổi từ I đến VII thời mới yên
Hoá trị II dùng rất nhiều
Hoá trị VII cũng được yêu hay cần
Bài ca hoá trị thuộc lòng
Viết thông công thức đề phòng lãng quên
Học hành cố gắng cần chuyên
Siêng ôn chăm luyện tất nhiên nhớ nhiều
V. Mở rộng
Bảng phiên âm tên gọi của 20 nguyên tố hóa học đầu
|
Số hiệu nguyên tử (Z) |
Kí hiệu hóa học |
Tên nguyên tố hóa học |
Phiên âm Quốc tế |
|
1 |
H |
Hydrogen |
/ˈhaɪdrədʒən/ |
|
2 |
He |
Helium |
/ˈhiːliəm/ |
|
3 |
Li |
Lithium |
/ˈlɪθiəm/ |
|
4 |
Be |
Beryllium |
/bəˈrɪliəm/ |
|
5 |
B |
Boron |
/ˈbɔːrɒn/ /ˈbɔːrɑːn/ |
|
6 |
C |
Carbon |
/ˈkɑːbən/ /ˈkɑːrbən/ |
|
7 |
N |
Nitrogen |
/ˈnaɪtrədʒən/ |
|
8 |
O |
Oxygen |
/ˈɒksɪdʒən/ /ˈɑːksɪdʒən/ |
|
9 |
F |
Fluorine |
/ˈflɔːriːn/ /ˈflʊəriːn/ /ˈflɔːriːn/ /ˈflʊriːn/ |
|
10 |
Ne |
Neon |
/ˈniːɒn/ /ˈniːɑːn/ |
|
11 |
Na |
Sodium |
/ˈsəʊdiəm/ |
|
12 |
Mg |
Magnesium |
/mæɡˈniːziəm/ |
|
13 |
Al |
Aluminium |
/ˌæljəˈmɪniəm/ /ˌæləˈmɪniəm/ /ˌæljəˈmɪniəm/ /ˌæləˈmɪniəm/ |
|
14 |
Si |
Silicon |
/ˈsɪlɪkən/ |
|
15 |
P |
Phosphorus |
/ˈfɒsfərəs/ /ˈfɑːsfərəs/ |
|
16 |
S |
Sulfur |
/ˈsʌlfə(r)/ /ˈsʌlfər/ |
|
17 |
Cl |
Chlorine |
/ˈklɔːriːn/ |
|
18 |
Ar |
Argon |
/ˈɑːɡɒn/ /ˈɑːrɡɑːn/ |
|
19 |
K |
Potassium |
/pəˈtæsiəm/ |
|
20 |
Ca |
Calcium |
/ˈkælsiəm/ |
Xêm thêm các bài viết liên quan hay, chi tiết khác:
30 bài tập về Cấu tạo của bảng tuần hoàn các nguyên tố hóa học (2024) có đáp án chi tiết nhất
30 Bài tập về Sơ lược về bảng tuần hoàn các nguyên tố hóa học (2024) có đáp án chi tiết nhất
30 bài tập xác định vị trí của các nguyên tố trong bảng tuần hoàn (2024) chi tiết, có đáp án
Cách xác định số thứ tự chu kì trong bảng tuần hoàn (2024) hay nhất, chi tiết nhất




