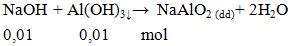Phản ứng Al(OH)3 + NaOH → NaAlO2 + H2O
1. Phương trình phản ứng Al(OH)3 tác dụng với NaOH
Al(OH)3 + NaOH → NaAlO2 + 2H2O
2. Điều kiện phản ứng Al(OH)3 ra NaAlO2
Nhiệt độ: 1000°C.
3. Cách tiến hành phản ứng Al(OH)3 tác dụng với NaOH
Cho dung dịch Al(OH)3 từ từ và ống nghiệm chứa sẵn dung dịch NaOH.
4. Hiện tượng phản ứng Al(OH)3 tác dụng với NaOH
Sản phẩm thu được chất rắn màu trắng.
5. Bản chất của các chất tham gia phản ứng
5.1. Bản chất của Al(OH)3 (Nhôm hidroxit)
Al(OH)3 là một hidroxit lưỡng tính nên có thể tác dụng được với axit mạnh và dung dịch có tính kiềm mạnh.
5.2. Bản chất của NaOH (Natri hidroxit)
NaOH là một bazơ mạnh nên tác dụng được với hợp chất lưỡng tính như Al(OH)3 hoặc Al2O3.
6. Mở rộng kiến thức về Nhôm hidroxit
6.1. Về tính chất vật lý
Al(OH)3 là một loại hợp chất hóa học dạng rắn, không tan được trong nước (ở bất cứ điều kiện nhiệt độ nào)
6.2. Tính chất hóa học của Al(OH)3
Kém bền với nhiệt: Khi đun nóng Al(OH)3 phân hủy thành Al2O3.
2Al(OH)3 Al2O3 + 3H2O
- Là hiđroxit lưỡng tính
Tác dụng với axit mạnh:
Al(OH)3 + 3HCl → AlCl3 + 3H2O
Tác dụng với dung dịch kiềm mạnh:
Al(OH)3 + KOH → KAlO2 + 2H2O
Al(OH)3 + KOH → K[Al(OH)4]
6.3. Cách điều chế nhôm hydroxit
Kết tủa ion Al3+
Phương trình hóa học: Al3+ + 3OH- (vừa đủ) → Al(OH)3
Phương trình hóa học: Al3+ + 3NH3 + 3H2O → Al(OH)3 + 3NH4+
Phương trình hóa học: 3NaOH + AlCl3 → 3NaCl + Al(OH)3
Kết tủa AlO2-:
Phương trình hóa học: AlO2- + CO2+ 2H2O → Al(OH)3 + HCO3-
Phương trình hóa học: AlO2- + H+ (vừa đủ) + H2O → Al(OH)3
Phương trình hóa học: NaAlO2+ CO2 + 2H2O → Al(OH)3 + NaHCO3
7. Bài tập vận dụng liên quan
Câu 1. Nhỏ từ từ cho đến dư dung dịch NaOH vào dung dịch AlCl3 hiện tượng xảy ra là
A. Có kết tủa keo trắng, sau đó kết tủa tan.
B. Chỉ có kết tủa keo trắng.
C. Có kết tủa keo trắng và khí bay lên.
D. Không có kết tủa, có khí bay lên.
Lời giải:
Nhỏ từ từ cho đến dư dung dịch NaOH vào dung dịch AlCl3, ban đầu có kết tủa keo trắng xuất hiện.
3NaOH + AlCl3→ Al(OH)3 ↓ + 3NaCl
Sau đó kết tủa keo trắng tan trong NaOH dư tạo dung dịch trong suốt (vì Al(OH)3 có tính lưỡng tính tan được trong dung dịch axit dư, và kiềm dư)
NaOH + Al(OH)3 → NaAlO2+ 2H2O
Câu 2. Các đồ vật bằng nhôm bền trong không khí và nước là do:
A. Có một lớp Al(OH)3 bên ngoài bảo vệ
B. Có một lớp Al2O3 bên ngoài bảo vệ
C. Nhôm không tan trong nước
D. Nhôm bền, không bị oxi hóa
Lời giải:
Nhôm bền trong môi trường không khí và nước là do có màng oxit Al2O3 bền vững bảo vệ
Khi nhôm tác dụng chậm với oxi và hơi nước, chúng tạo thành một lớp nhôm oxit (Al2O3).
Lớp nhôm oxit này bám rất chắc vào bề mặt nhôm. Và ngăn chặn hoàn toàn không cho oxi tác dụng trực tiếp với nhôm. Do đó, nhôm bền trong môi trường không khí là nhờ lớp bảo vệ nhôm oxit ngay cả khi đun nóng
Câu 3. Chất nào dưới đây có thể tác dụng được với HCl và dung dịch NaOH
A. CuO
B. Fe(OH)3
C. Al(OH)3
D. Al(NO3)3
Lời giải:
Phương trình phản ứng xảy ra
Al(OH)3 + NaOH → NaAlO2 + 2H2O
Al(OH)3 + 3HCl → AlCl3+ 3H2O
Câu 4. Dãy các chất đều phản ứng được với kim loại nhôm là:
A. O2, Cl2, NaOH
B. O2, Cl2, Mg(OH)2
C. O2, S, HNO3 đặc, nguội
D. O2, S, MgCl2
Lời giải:
Câu 5. Dãy chất nào dưới đây phản ứng được NaOH?
A. Al2O3; Al(OH)3; NaNO3
B. Al2O3; Fe, Al(OH)3
C. Al(NO3)3, HCl, CO2
D. FeCl3, Ag, CO2
Lời giải:
Phương trình phản ứng liên quan
Al(NO3)3 + 3NaOH → Al(OH)3 + 3NaNO3
NaOH + HCl → NaCl + H2O
CO2 + NaOH → Na2CO3 + H2O
Câu 6. Thổi V lít khí CO2 (đktc) vào 100ml dd Ca(OH)2 1M thu được 6 gam kết tủa. Lọc kết tủa đun nóng dd lại thấy có kết tủa nữa. Tìm V?
A. 1,08 lít
B. 3,136 lít
C. 2,24 lít
D. 3,36 lít
Lời giải:
nkết tủa = 6100= 0,06 mol
Vì đun nóng lại thu được kết tủa nên dd thu được 2 muối: CaCO3; Ca(HCO3)2.
Phương trình hóa học
CO2+ Ca(OH)2 → CaCO3 + H2O
0,06
2CO2 + Ca(OH)2 → Ca(HCO3)2.
0,08 0,04
→ n(CO2) = 0,06 + 0,08 = 0,14. → V = 3,136 lít.
Câu 7. Phát biểu nào dưới đây là sai ?
A. Cho từng viên Na vào dung dịch AlCl3, xảy ra hiện tượng Natri tan, sủi bọt khí, có xuất hiện kết tủa keo trắng, sau đó kết tủa tan
B. Al(OH)3, Al2O3, Al đều là các chất lưỡng, tính
C. Nhôm là kim loai nhẹ và có khả năng dẫn điện Iot
D. Từ Al2O3 có thế điều chế được Al.
Lời giải:
A-Đúng vì đầu tiên Na tác dụng với nước, tan và tạo bọt khí, sau đó tạo kết tủa Al(OH)3, khi Na dư kết tủa sẽ tan
B-Sai vì chỉ có Al(OH)3, Al2O3, là các chất lưỡng, tính còn Al không phải là chất lưỡng tính
C-Đúng
D-Đúng
Câu 8. Số mol NaOH cần dung để phản ứng hoàn toàn với 0,78g Al(OH)3 là
A. 0,001.
B. 0,01.
C. 0,1.
D. 1.
Lời giải:
Đáp án: B
Câu 9. Phát biểu nào dưới đây đúng trong các câu sau:
A. Nhôm là kim loại lưỡng tính.
B. Al(OH)3 là một bazo lưỡng tính có thể tác dụng HCl và NaOH
C. Al(OH)3 là một hidroxit lưỡng tính có thể tác dụng HCl và NaOH
D. Al2O3 là oxit trung tính.
Lời giải:
A-Sai vì Nhôm không phải là kim loại lưỡng tính.
B-Sai Al(OH)3 là một hidroxit lưỡng tính có thể tác dụng HCl và NaOH
C-Đúng
D-Sai Al2O3 là oxit lưỡng tính
Câu 10. Nhôm bị thụ động trong dung dịch nào sau đây
A. H2SO4 đặc nóng
B. HNO3 đặc nguội
C. H2SO4 loãng
D. HNO3 đặc nóng
Lời giải:
Nhôm bị thụ động trong dung dịch: HNO3 đặc nguội
Câu 11. Phản ứng nào sau đây không là phản ứng trao đổi?
A. NaOH + Al(OH)3 → NaAlO2+ 2H2O
B. 2NaOH + FeSO4 → Na2SO4 + Fe(OH)2 ↓
C. 2NaOH + CuSO4 → Na2SO4 + Cu(OH)2 ↓
D. 2KOH + MgSO4 → K2SO4 + Mg(OH)2 ↓
Lời giải:
Đáp án: A
NaOH + Al(OH)3 → NaAlO2+ 2H2O không là phản ứng trao đổi.
Câu 12. Cho các thí nghiệm sau:
(1). Sục khí CO2 vào dung dịch natri aluminat.
(2). Cho dung dịch NH3 dư vào dung dịch AlCl3 .
(3). Sục khí H2S vào dung dịch AgNO3.
(4). Dung dịch NaOH dư vào dung dịch AlCl3.
(5). Dung dịch NaOH dư vào dung dịch Ba(HCO3)2.
Những trường hợp thu được kết tủa sau phản ứng là:
A. (1), (2), (5)
B. (2), (3), (4), (5)
C. (2), (3), (5)
D. (1), (2), (3), (5)
Lời giải:
(1). Sục khí CO2 vào dd natri aluminat.
2H2O + NaAlO2 + CO2 → Al(OH)3 + NaHCO3
(2). Cho dung dịch NH3 dư vào dd AlCl3:
AlCl3 + 3H2O + 3NH3 → Al(OH)3↓ + 3NH4Cl
(3). Sục khí H2S vào dd AgNO3.
2AgNO3 + H2S → 2HNO3 + Ag2S
(4). Dung dịch NaOH dư vào dd AlCl3. Không có kết tủa vì bị tan
AlCl3 + 3NaOH → Al(OH)3↓ + 3NaCl
Al(OH)3 + NaOH → NaAlO2 + 2H2O
(5). Dung dịch NaOH dư vào dd Ba(HCO3)2.
2NaOH + Ba(HCO3)2 → 2H2O + Na2CO3 + BaCO3 ↓
Câu 13. Kim loại vừa tác dụng với dung dịch HCl vừa tác dụng với dung dịch KOH là:
A. Fe
B. Mg
C. Na
D. Al
Lời giải:
Al vừa tác dụng với dung dịch HCl vừa tác dụng với dung dịch NaOH
Phương trình hóa học
2Al + 6HCl → 2AlCl3 + 3H2↑
Al + NaOH + H2O → NaAlO2 + 32H2↑
Câu 14. Cho các kim loại: Cu, Zn, Fe, Mg, Ag, Al. Những kim loại nào không tác dụng với dd HNO3 đặc nguội?
A. Fe, Mg, Ag, Al.
B. Cu, Mg, Ag, Al.
C. Fe, Al.
D. Tất cả các kim loại
Lời giải:
2 kim loại không phản ứng với dung dịch HNO3 đặc nguội là Fe và Al
Câu 15. Cho 4,005 g AlCl3 vào 1000 ml dung dịch NaOH 0,1M. Sau khi phản ứng xong thu được khối lượng kết tủa là
A. 1,56 g;
B. 2,34 g;
C. 2,60 g;
D. 1,65 g.
Lời giải:
Lời giải:
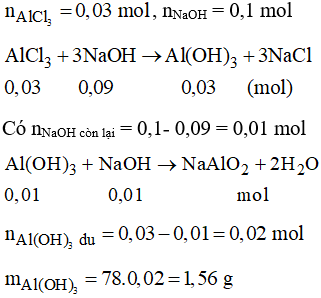
Câu 16. Tiến hành các thí nghiệm sau :
(a) Cho dd AgNO3 vào dd HCl
(b) Cho Al2O3 vào dung dịch HCl loãng dư
(c) Cho Cu vào dung dịch HCl đặc nóng dư
(d) Cho Ba(OH)2 vào dung dịch KHCO3
Sau khi phản ứng kết thúc, số thí nghiệm thu được chất rắn là
A. 4
B. 2
C. 5
D. 3
Lời giải:
(a) đúng tạo AgCl
(b) sai vì Al2O3 tan hết trong HCl
(c) đúng vì Cu không tác dụng với HCl nên còn nguyên sau phản ứng
(d) đúng do tạo kết tủa BaCO3 : Ba(OH)2+KHCO3→BaCO3+KOH+H2O
Vậy có 3 thí nghiệm thu được chất rắn sau phản ứng.
Câu 17. Hoà tan hoàn toàn m gam AlCl3 vào nước được dung dịch X. Nếu cho 480 ml dung dịch NaOH 1M vào X thì thu được 4a gam kết tủa. Mặt khác, nếu cho 170 ml dung dịch NaOH 3M vào X thì thu được 3a gam kết tủa. Giá trị của m là
A. 14,685
B. 21,36
C. 20,025
D. 16,02
Lời giải:
TH1: Khi cho 0,48 mol NaOH thì chỉ tạo 1 phần kết tủa, khi cho 0,51 mol NaOH thì tạo kết tủa tối đa vào 1 phần bị tanTrường hợp cho 0,51 mol NaOH
TH2: cả 2 lần đều tạo kết tủa tối đa và hòa tan 1 phần
Chênh lệch số mol kết tủa ở 2 trường hợp:4a78
Trường hợp cho 0,48 mol NaOH
Câu 18. Nhỏ từ từ dung dịch NaOH đến dư vào ống nghiệm chứa Al(NO3)3. Hiện tượng thu được sau phản ứng là
A. xuất hiện kết tủa keo trắng.
B. xuất hiện kết tủa màu nâu đỏ.
C. xuất hiện kết tủa keo trắng, sau đó kết tủa tan.
D. xuất hiện kết tủa keo xanh.
Lời giải:
Đáp án: C
3NaOH + Al(NO3)3 → 3NaNO3+ Al(OH)3 ↓
Al(OH)3: kết tủa keo trắng , sao đó NaOH dư, kết tủa tan theo phương trình:
NAOH + Al(OH)3 ↓ → KAlO2 (dd)+ 2H2O
Câu 19. Cho sơ đồ phản ứng sau: Al → X → Y → Al(OH)3. Trong sơ đồ trên, mỗi mũi tên là một phản ứng, các chất X, Y lần lượt là
A. NaAlO2 và Al(OH)3
B. Al2O3 và Al(NO3)3
C. Al(OH)3 và Al2O3
D. Al(OH)3 và Al(NO3)3
Lời giải:
Phương trình phản ứng hóa học
4Al + 3O2 → 2Al2O3
Al2O3 + 6HNO3 → 2Al(NO3)3 + 3H2O
Al(NO3)3 + 3NH3+ 3H2O → Al(OH)3 + 3NH4NO3
Câu 20. Criolit (còn gọi là băng thạch) có công thức phân tử Na3AlF6, được thêm vào Al2O3 trong quá trình điện phân Al2O3 nóng chảy để sản xuất nhôm. Cho các tác dụng sau:
(1) Bảo vệ điện cực khỏi bị ăn mòn.
(2) Làm tăng độ dẫn điện của Al2O3 nóng chảy
(3) Làm giảm nhiệt độ nóng chảy của Al2O3
(4) Tạo lớp ngăn cách để bảo vệ Al nóng chảy
Tác dụng của Criolit là đúng
A. (1), (2), (3), (4)
B. (1), (2), (3)
C. (2), (3), (4)
D. (1), (2), (4)
Lời giải:
(2) Làm tăng độ dẫn điện của Al2O3 nóng chảy
(3) Làm giảm nhiệt độ nóng chảy của Al2O3
(4) Tạo lớp ngăn cách để bảo vệ Al nóng chảy
Xem thêm các phương trình khác:
NH3 + AlCl3 + H2O → Al(OH)3 + NH4Cl | NH3 ra NH4Cl
Al4C3 + H2O → CH4 + Al(OH)3 | Al4C3 ra CH4
Al4C3 ra CH4 l Al4C3 + H2O → CH4 + Al(OH)3 | Nhôm cacbua ra Metan
Al + H2O + NaOH → NaAlO2 + H2 | Al ra NaAlO2
Al2O3 + NaOH → NaAlO2 + H2O | Al2O3 ra NaAlO2