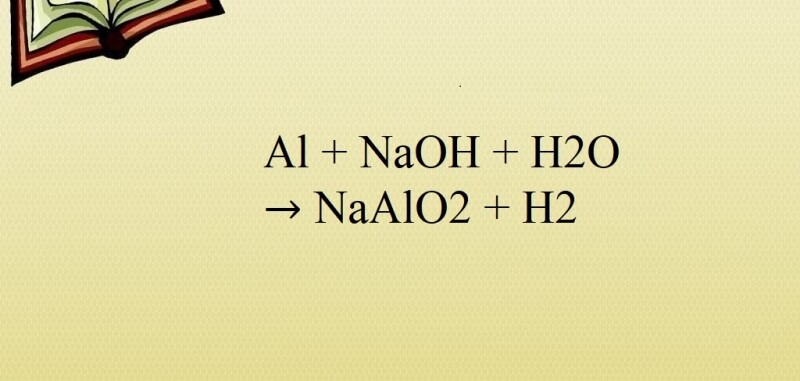
Phản ứng Al + H2O + NaOH → NaAlO2 + H2
1. Phương trình phản ứng Al tác dụng với NaOH
2Al + 2H2O + 2NaOH → 2NaAlO2 + 3H2↑
2. Điều kiện phản ứng Al ra NaAlO2
Nhiệt độ: Từ 400oC - 500oC
3. Phương trình ion rút gọn khi cho Al tác dụng NaOH
Phương trình phân tử
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
Phương trình ion rút gọn
2Al + 2H2O + 2OH- → 2AlO2- + 3H2
4. Cách tiến hành phản ứng cho Al tác dụng với NaOH
Cho đồng Al tác dụng với dung dịch bazo NaOH.
5. Hiện tượng Hóa học
Kim loại Al tan dần trong dung dịch và xuất hiện bọt khí, khí thoát ra chính là hidro H.
Bản chất của phản ứng nhôm tác dụng với dung dịch kiềm như sau: Ở điều kiện bình thường nhôm có lớp oxit Al2O3 rất mỏng, bền và mịn bảo vệ nhôm nên nhôm không tác dụng với nước. Khi nhôm tiếp xúc với dung dịch kiềm thì lớp oxit Al2O3 này sẽ bị kiềm hòa tan, khi đó nhôm không còn màng oxit bảo vệ, nhôm sẽ tác dụng với nước theo phương trình sau:
2Al + 6H2O → 2Al(OH)3↓+ 3H2↑ (1)
Al(OH)3 tác dụng tiếp với dung dịch kiểm theo phương trình:
Al(OH)3 + NaOH → NaAlO2 + H2O (2)
Vậy phản ứng nhôm tan trong dung dịch kiểm là sự tổng hợp của phương trình (1),(2) và giải phóng khí H2:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
6. Tính chất hóa học của nhôm
6.1. Tác dụng với oxi và một số phi kim.
4Al + 3O2→ 2Al2O3
ở điều kiện thường, nhôm phản ứng với oxi tạo thành lớp Al2O3 mỏng bền vững, lớp oxit này bảo vệ đồ vật bằng nhôm, không cho nhôm tác dụng oxi trong không khí, nước.
2Al + 3Cl2 → 2AlCl3
6.2. Nhôm tác dụng với axit (HCl, H2SO4 loãng,..)
- Tác dụng với axit (HCl, H2SO4 loãng,..)
2Al + 6HCl → 2AlCl3 + 3H2
Chú ý: Nhôm không tác dụng với H2SO4, HNO3 đặc, nguội
- Tác dụng với axit có tính oxi hóa mạnh như HNO3 hoặc H2SO4 đậm đặc
Al + 4HNO3→ Al(NO3)3 + NO + 2H2O
Al + 6HNO3 → Al(NO3)3 + 3NO2 + 3H2O
2Al + 6H2SO4 → Al2(SO4)3 + 3SO2 + 6H2O
6.3. Tác dụng với dung dịch muối của kim loại yếu hơn.
AI + 3AgNO3 → Al(NO3)3 + 3Ag
2Al + 3FeSO4 → Al2(SO4)3 + 3Fe
6.4. Tính chất hóa học riêng của nhôm.
Do lớp oxit nhôm bị hòa tan trong kiềm nên nhôm phản ứng với dung dịch kiềm.
2Al + 2H2O + 2NaOH → 2NaAlO2+ 3H2↑
6.5. Phản ứng nhiệt nhôm.
Phản ứng nhiệt nhôm là phản ứng hóa học toả nhiệt trong đó nhôm là chất khử ở nhiệt độ cao.
Ví dụ nổi bật nhất là phản ứng nhiệt nhôm giữa oxit sắt III và nhôm:
Fe2O3+ 2Al → 2Fe + Al2O3
Một số phản ứng khác như:
3CuO+ 2Al → Al2O3 + 3Cu
8Al + 3Fe3O4 → 4Al2O3 + 9Fe
7. Bài tập vận dụng liên quan
Câu 1. Nhận định nào sau đây sai về tính chất vật lí của nhôm?
A. Nhôm là kim loại nhẹ, dẫn nhiệt tốt.
B. Nhôm là kim loại màu trắng bạc, có ánh kim.
C. Nhôm dẫn điện tốt hơn đồng.
D. Nhôm có tính dẻo dễ kéo sợi.
Lời giải:
A đúng vì nhôm là kim loại nhẹ, dẫn nhiệt tốt.
B đúng vì nhôm là kim loại màu trắng bạc, có ánh kim.
C sai vì nhôm có độ dẫn điện bằng 23 độ dẫn điện đồng (dẫn điện kém hơn đồng).
D đúng nhôm có tính dẻo dễ kéo sợi
Câu 2. Nhôm không tan trong dung dịch nào sau đây?
A. HCl.
B. H2SO4.
C. NaHSO4.
D. NH3.
Lời giải:
Phương trình phản ứng minh họa
2Al + 6HCl → 2AlCl3 + 3H2
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
2Al + 6NaHSO4 → 3Na2SO4 + Al2(SO4)3 + 3H2
Câu 3. Chất nào sau đây tác dụng với dung dịch NaAlO2 thu được kết tủa?
A. khí CO2.
B. dung dịch NaOH.
C. dung dịch Na2CO3.
D. dung dịch HCl dư.
Lời giải:
Phương trình phản ứng minh họa
NaAlO2 + CO2 + 2H2O → Al(OH)3↓+ NaHCO3
NaAlO2 + HCl + H2O → NaCl + Al(OH)3↓
Al(OH)3 + 3HCl (dư) → AlCl3 + 3H2O
Câu 4. Cho 2,7 gam Al tan hoàn toàn trong dung dịch NaOH, sau phản ứng thu được V lít thoát ra. Giá trị của V ở điều kiện tiêu chuẩn là:
A. 6,72 lít
B. 2,24 lít
C. 3,36 lít
D. 4,48 lít
Lời giải:
nAl = 0,1 mol
Phương trình phản ứng hóa học
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
0,1 mol → 0,15 mol
VH2 = 0,15.22,4 = 3,36 lít
Câu 5. Rót 100ml dung dịch NaOH 3,5M vào 100 ml dung dịch AlCl3 1M thu được m gam kết tủa. Tính m?
A. 3,9 gam
B. 1,95 gam
C. 7,8 gam
D. 11,7 gam
Lời giải:
nNaOH= 0,35 mol
nAlCl3= 0,1 mol
Phương trình phản ứng hóa học
AlCl3+ 3NaOH → Al(OH)3 + 3NaCl
=> NaOH dư 0,05 mol. Tạo 0,1 mol Al(OH)3
Vì dư kiềm nên Al(OH)3 tan 1 phần
Al(OH)3 + NaOH → NaAlO2+ 2H2O
=> nAl(OH)3 tan= 0,05 mol
=> nAl(OH)3 dư= 0,1 - 0,05= 0,05 mol
=> mAl(OH)3 dư= 3,9g
Câu 6. Cho các nhận định sau:
(1) Nhôm là kim loại nhẹ, dễ dát mỏng, có tính khử mạnh, dẫn điện, dẫn nhiệt tốt.
(2) Các kim loại kiềm thổ tác dụng được với nước ở điều kiện thường.
(3) Các kim loại kiềm và kiềm thổ được điều chế bằng phương pháp điện phân nóng chảy muối halogen.
(4) Thành phần cacbon trong gang trắng nhiều hơn trong gang xám.
(5) Trong công nghiệp, crom được dùng để sản xuất và bảo vệ thép.
(6) Phèn chua được dùng trong ngành thuộc da, chất cầm màu trong công nghiệp nhuộm vải.
(7) Các kim loại kiềm dễ cháy trong oxi khi đốt, chỉ tạo thành các oxit.
(8) Ở nhiệt độ cao, các kim loại đứng trước H đều khử được H2O.
Số nhận định đúng là:
A. 3
B. 5
C. 4
D. 6
Lời giải:
Cho các nhận định sau:
(1) Đúng Nhôm là kim loại nhẹ, dễ dát mỏng, có tính khử mạnh, dẫn điện, dẫn nhiệt tốt.
(2) Sai vì Mg, Be không tác dụng được với nước ở nhiệt độ thường
(3) Đúng Các kim loại kiềm và kiềm thổ được điều chế bằng phương pháp điện phân nóng chảy muối halogen.
Kim loại kiềm kiềm thổ và nhôm có thể được điều chế bằng phương pháp điện phân nóng chảy.
Các kim loại kiềm và kiềm thổ được điều chế bằng phương pháp điện phân nóng chảy muối halogen.
(4) Đúng
Gang xám: Chủ yếu, thành phần của gang xám là; khoảng 2,5% đến 4,0% cacbon, 1% đến 3% silic và phần còn lại cân bằng sử dụng sắt.
Gang trắng: Nói chung, gang trắng chủ yếu chứa cacbon và silic; khoảng 1,7% đến 4,5% cacbon và 0,5% đến 3% silic.
(5) Trong công nghiệp, crom được dùng để sản xuất và bảo vệ thép.
(6) Đúng
Phèn chua được dùng trong ngành công nghiệp thuộc da, công nghiệp giấy, chất cầm màu trong ngành nhuộm vải, chất làm trong nước. Công thức hoá học của phèn chua là K2SO4.Al2(SO4)3.24H2O.
(7) Các kim loại kiềm dễ cháy trong oxi khi đốt, chỉ tạo thành các oxit.
(8) Ở nhiệt độ cao, các kim loại đứng trước H đều khử được H2O.
Câu 7. Nhận định không chính xác về nhôm là:
A. Nhôm là kim loại nhẹ, dễ dát mỏng.
B. Nhôm là kim loại có tính khử tương đối mạnh.
C. Trong công nghiệp, nhôm được điều chế bằng phương pháp điện phân nóng chảy.
D. Nhôm có thể khử được các oxit của kim loại kiềm.
Lời giải:
Nhận định không chính xác về nhôm là: Nhôm có thể khử được các oxit của kim loại kiềm.
Câu 8. Cho các nhận định sau, nhận định nào đúng
(1) Nhôm là chất rắn màu trắng, nhẹ, có ánh kim
(2) Nhôm dẫn điện , dẫn nhiệt kém
(3) Nhôm dễ dát mỏng, kéo sợi
(4) Nhôm dẫn nhiệt tốt nên được dùng làm nồi, xoong nấu ăn
(5) Điều chế nhôm bằng phương pháp điện phân nóng chảy
A. (1), (2), (3)
B. (1), (3), (4), (5)
C. (3),(4),(5)
D. (2), (4), (5)
Lời giải:
1) Nhôm là chất rắn màu trắng, nhẹ, có ánh kim => đúng
(2) Nhôm dẫn điện , dẫn nhiệt kém => sai
(3) Nhôm dễ dát mỏng, kéo sợi => đúng
(4) Nhôm dẫn nhiệt tốt nên được dùng làm nồi, xoong nấu ăn => đúng
(5) Điều chế nhôm bằng phương pháp điện phân nóng chảy => đúng
Câu 9. Hòa tan hết a mol Al vào dung dịch chứa 2a mol NaOH thu được dung dịch X. Kết luận nào sau đây đúng
A. Sục CO2 dư vào dung dịch X thu được a mol kết tủa.
B. Dung dịch X không phản ứng với dung dịch CuSO4.
C. Thêm 2a mol HCl vào dung dịch X thu được 2a3 mol kết tủa.
D. Dung dịch X làm quỳ tím chuyển sang màu đỏ.
Lời giải:
Phương trình phản ứng hóa học
Al + 2H2O + 2NaOH → 3H2 + 2NaAlO2
a a a (mol)
Dung dịch X gồm: NaOH dư (a mol) và NaAlO2 (a mol)
A. 2H2O + NaAlO2 + CO2 → Al(OH)3 + NaHCO3
a a a (mol)
NaOH + CO2 → Na2CO3
B. CuSO4 + NaOH → Cu(OH)2 + Na2SO4
C. HCl + NaOH → NaCl + H2O
a a (mol)
H2O + HCl + NaAlO2 → Al(OH)3 + NaCl
a a a (mol)
D. dung dịch X chứa NaOH dư do đó làm quỳ hóa xanh
Câu 10. Hòa tan m gam hỗn hợp X gồm Al và Na có tỉ lệ mol 1:2 vào nước dư thu được 4,48 lít khí (đktc). Giá trị của m là
A. 5,84.
B. 6,15.
C. 7,30.
D. 3,65.
Lời giải:
Gọi nAl = x (mol)
=> nNa = 2x (mol)
nH2 = 4,4822,4 = 0,2 (mol)
Phương trình phản ứng hóa học
Na + H2O → NaOH + 0,5H2↑
2x → x (mol)
Al + NaOH + H2O → NaAlO2 + 1,5H2↑
x → 1,5x (mol)
Vì Na : Al có tỉ lệ 1: 2 nên cả Na và Al cùng phản ứng hết
=> nH2 = x + 1,5x = 0,2
=> x = 0,08 (mol)
=> m = 0,08.27 + 2.0,08.23 = 5,84 (g)
Câu 11. Dãy chất nào dưới đây tác dụng với nhôm (dạng bột) là:
A. O2, dung dịch Ba(OH)2, dung dịch HCl.
B. Dung dịch Na2SO4, dung dịch NaOH, Cl2
C. H2, I2, dung dịch HNO3 đặc nguội, dung dịch FeCl3
D. Dung dịch FeCl3, H2SO4 đặc nguội, dung dịch KOH
Lời giải:
Al không phản ứng với dung dịch HNO3 đặc nguội, H2SO4 đặc nguội, Dung dịch Na2SO4 nên => B, C, D sai
Phương trình phản ứng minh họa
4Al + 3O2→ 2Al2O3
2Al + Ba(OH)2 + 2H2O → Ba(AlO2)2+ 3H2
2Al + 6HCl → 2AlCl3 + 3H2
Câu 12. Dãy các chất nào sau đây khi phản ứng với HNO3 đặc nóng đều tạo khí:
A. Cu(OH)2, FeO, C
B. Fe3O4, C, FeCl2
C. Na2O, FeO, Ba(OH)2
D. Fe3O4, C, Cu(OH)2
Lời giải:
Phương trình phản ứng minh họa
Fe3O4 + 10HNO3 → 3Fe(NO3)3+ NO2 + 5H2O
C + 4HNO3→ CO2 + 4NO2 + 2H2O
3FeCl2 + 10HNO3 → 3Fe(NO3)3 + NO + 2H2O + 6HCl
Câu 13. Thí nghiệm nào sau đây có kết tủa sau phản ứng?
A. Cho dung dịch NH3 đến dư vào dung dịch AlCl3
B. Cho dung dịch NaOH đến dư vào dung dịch Cr(NO3)3
C. Thổi CO2 đến dư vào dung dịch Ba(OH)2
D. Cho dung dịch HCl đến dư vào dung dịch NaAlO2
Lời giải:
B. Cho dung dịch NaOH đến dư vào dung dịch Cr(NO3)3.
NaOH + Cr(NO3)3 → Cr(OH)3+ NaNO3
Cr(OH)3 + NaOH → NaCrO2+ H2O
C. Thổi CO2 đến dư vào dung dịch Ba(OH)2.
CO2+ Ba(OH)2 → CaCO3 + H2O
CO2 + BaCO3 + H2O → Ca(HCO3)2.
D. Cho dung dịch HCl đến dư vào dung dịch NaAlO2.
NaAlO2 + HCl + H2O → Al(OH)3+ NaCl
Al(OH)3 + 3HCl → AlCl3 + 3H2O.
A. Cho dung dịch NH3 đến dư vào dung dịch AlCl3.
AlCl3 + 3NH3+ H2O → Al(OH)3 + 3NH4Cl
Nên thí nghiệm có kết tủa sau phản ứng: Cho dung dịch NH3 đến dư vào dung dịch AlCl3.
Câu 14. Chọn nhận định sai:
A. HNO3 là chất lỏng, không màu, tan có giới hạn trong nước.
B. N2O5 là anhiđrit của axit nitric
C. Dung dịch HNO3 có tính oxi hoá mạnh do có ion NO3-
D. HNO3 là axit mạnh.
Lời giải:
HNO3 là chất lỏng, không màu, tan có giới hạn trong nước.
Câu 15. Cho một lá nhôm vào ống nghiệm chứa dung dịch Hg(NO3)2, thấy có một lớp thủy ngân bám trên bề mặt nhôm. Hiện tượng tiếp theo quan sát được là:
A. khí hiđro thoát ra mạnh.
B. khí hiđro thoát ra sau đó dừng lại ngay.
C. lá nhôm bốc cháy.
D. lá nhôm tan ngay trong thủy ngân và không có phản ứng.
Lời giải:
Phương trình phản ứng có thể xảy ra
2Al + 3Hg(NO3)2 → 2Al(NO3)3 + 3Hg
Al sẽ tạo với Hg hỗn hống. Hỗn hống Al tác dụng với nước
2Al + 6H2O → 2Al(OH)3 + 3H2
Câu 16. Thực hiện các thí nghiệm sau :
(a) Cho từ từ NaOH đến dư vào dung dịch Al2(SO4)3,
(b) Cho từ từ Al2(SO4)3 đến dư vào dung dịch NaOH,
(c) Cho từ từ NH3 đến dư vào dung dịch Al2(SO4)3,
(d) Cho từ từ Al2(SO4)3 đến dư vào dung dịch NH3.
(e) Cho từ từ HCl đến dư vào dung dịch NaAlO2.
(f) Cho từ từ NaAlO2 đến dư vào dung dịch HCl
(g) Cho từ từ Al2(SO4)3 đến dư vào dung dịch NaAlO2
Trong các thí nghiệm trên, số thí nghiệm xuất hiện kết tủa là
A. 2.
B. 3.
C. 5.
D. 7.
Lời giải:
a) Xuất hiện kết tủa màu trắng, lượng kết tủa tăng dần đến cực đại và sau đó kết tủa tan ra cho đến hết, dung dịch trở nên trong suốt.
Al2(SO4)3 + 6NaOH → 2Al(OH)3 + 3Na2SO4;
Al(OH)3 + NaOH → NaAlO2 + 2H2O.
b) Xuất hiện kết tủa màu trắng
Al2(SO4)3 + 6NaOH → 2Al(OH)3 + 3Na2SO4
c) Có kết tủa keo trắng xuất hiện.
Al2(SO4)3 + 6NH3 + 6H2O → 2Al(OH)3 + 3(NH4)2SO4
d) Có kết tủa keo trắng xuất hiện.
Al2(SO4)3 + 6NH3 + 6H2O → 2Al(OH)3 + 3(NH4)2SO4
e) Ban đầu: NaAlO2+ HCl + H2O → Al(OH)3↓ + NaCl.
Sau đó, Al(OH)3 ↓ + 3HCl → AlCl3 + 3H2O
f) Có kết tủa trắng xuất hiện
NaAlO2 + HCl + H2O → Al(OH)3↓ + NaCl
g) Có kết tủa trắng xuất hiện
Al2(SO4)3 + 6NaAlO2 + 12H2O → 8Al(OH)3 + 3Na2SO4
Câu 17. Cho m gam hỗn hợp X gồm 2 kim loại kiềm thuộc 2 chu kì liên tiếp tác dụng với 180 ml dung dịch Al2(SO4)3 1M thu được 15,6 gam kết tủa; khí H2 và dung dịch A. Nếu cho m gam hỗn hợp X tác dụng với 240 gam dung dịch HCI 18,25% thu được dung dịch B và H2. Cô cạn dung dịch B thu được 83,704 gam chất rắn khan. Biết rằng m < 45 gam. Phần trăm khối lượng của kim loại kiềm có nguyên tử khối nhỏ hơn trong X là:
A. 48,57%.
B. 37,10%.
C. 16,43%.
D. 28,22%.
Lời giải:
Đặt công thức chung của 2 kim loại là X : nAl3+ = 0,36 mol; nAl(OH)3 = 0,2 mol
Trường hợp 1: OH- phản ứng với Al3+ dư:
nOH- = 3n↓ = 0,6 = nX
Trường hợp 2: OH- dư phản ứng Al3+
nOH- = 3nAl3+ + (nAl3+ - n↓) = 1,24 = nX
Nếu nX = 0,6 < nHCl ⇒ 83,704 gam muối XCl
⇒ nCl- = 0,6 mol hay mCl- = 21,3 gam ⇒ mX = 62,404 gam > 45(loại)
Nếu nX = 1,24 mol > nHCl ⇒ 83,704 gam gồm muối XCl (1,2 mol) và XOH (0,04 mol)
⇒ mX = 40,424 < 45 . Ta có: X = 32,6
Hai kim loại kiềm là Na và K
Tính được số mol Na và K lần lượt là 0,496 và 0,744
%mNa = 28,22%
Câu 18. Dùng hóa chất nào sau đây để phân biệt Zn(NO3)2 và Al(NO3)3?
A. Dung dịch NaOH
B. Dung dịch Ba(OH)2
C. Dung dịch NH3
D. Dung dịch nước vôi trong
Lời giải:
Khi cho NH3 vào 2 dung dịch cả 2 dung dịch đều xuất hiện kết tủa hidroxit, nhưng Zn(OH)2 tạo thành có khả năng tạo phức với NH3 nên kết tủa lại tan, còn với Al(OH)3 không tan trong NH3
Al3+ tạo kết tủa keo trắng Al3++ 3NH3 + 3H2O → Al(OH)3 + 3NH4+
Zn2+ tạo kết tủa tan trong NH3 dư, Zn2+ + 2NH3 + 2H2O → Zn(OH)2 + 2NH4+
Zn(OH)2 + 4NH3 → (Zn(NH3)4)(OH)2
Câu 19. Câu nào dưới đây nói đúng về tính chất vật lí của nhôm
A. Màu trắng bạc, nhẹ, có ánh kim, dẫn điện và dẫn nhiệt tốt.
B. Màu trắng bạc nặng, có ánh kim, dẫn điện và dẫn nhiệt tốt.
C. Màu trắng xám, nhẹ, có ánh kim, dẫn điện và nhiệt kém.
D. Màu trắng xám, nặng, có ánh kim, dẫn điện và nhiệt kém.
Lời giải:
Tính chất vật lí của nhôm: Màu trắng bạc, nhẹ, có ánh kim, dẫn điện và dẫn nhiệt tốt.
Câu 20. Cho 0,51 gam oxit của một kim loại có công thức là M2O3 tác dụng vừa đủ 300 ml dung dịch HCl 0,1M. Công thức oxit đó.
A. Fe2O3
B. Al2O3
C. Cr2O3
D. Mn2O3
Lời giải:
nHCl = 0,3.0,1 = 0,03 mol
Phương trình phản ứng tổng quát
M2O3 + 6HCl → 2MCl3 + 3H2O
x mol 6 mol
Ta có: 6x = 0,03 => x = 0,005 mol
=> MM2O3 = 0,510,005 = 102 (g/mol) => MM = 102-3.122 = 27 (g/mol)
Câu 21. Thả một mẩu nhôm vào ống nghiệm chứa dung dịch CuSO4. Sau phản ứng quan sát được hiện tượng gì:
A. Không có dấu hiệu phản ứng.
B. Có chất rắn màu trắng bám ngoài lá nhôm, màu xanh của dung dịch CuSO4 nhạt dần.
C. Có chất rắn màu đỏ bám ngoài lá nhôm, màu xanh của dung dịch CuSO4 nhạt dần.
D. Có chất khí bay ra, dung dịch không đổi màu
Lời giải:
Phương trình phản ứng minh họa
2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
→ Có chất rắn màu đỏ bám ngoài lá nhôm, màu xanh của dung dịch CuSO4 nhạt dần.
Câu 22. Cho 700 ml dung dịch KOH 0,1M vào 100 ml dung dịch AlCl3 0,2M. Sau phản ứng khối lượng kết tủa tạo ra là:
A. 0,78 (g)
B. 1,56 (g)
C. 0,39 (g)
D. 0,26 (g)
Lời giải:
Theo bài ra ta có: nKOH = 0,7.0,1 = 0,07 (mol);
nAlCl3 = 0,1.0,2 = 0,02 (mol).
Ta có phương trình phản ứng hóa học sau:
AlCl3 + 3KOH → Al(OH)3 + 3KCl
Ban đầu: 0,02 0,07 mol
Phản ứng: 0,02 0,06 0,02 0,06
Sau phản ứng: 0 0,01 0,02 0,06
Vì vậy KOH còn dư nên ta có phản ứng:
Al(OH)3 + KOH → 2H2O + KAlO2
Ban đầu: 0,02 0,01
Phản ứng: 0,01 ← 0,01
Sau phản ứng: 0,01 0 0,01
Vậy sau khi xảy ra phản ứng hoàn toàn, ta có:
nKAlO2= 0,01 (mol) và nAl(OH)3 = 0,01 (mol)
⇒ mAl(OH)3 = 0,01.78 = 0,78 (g).
Câu 23. Cho 0,5 lít dung dịch NaOH tác dụng với 300ml dung dịch Al2(SO4)3 0,2M thu được 1,56g kết tủa. Tính nồng độ mol/lit của dung dịch NaOH biết các phản ứng xảy ra hoàn toàn.
A. 0,12M
B. 0,12M hoặc 0,92M
C. 0,92M
D. 0,15M hoặc 0,92M
Lời giải:
nAl3+ = 0,12 mol; n↓ = 0,02 mol.
Ta thấy n↓ < nAl3+ và bài không yêu cầu tính lượng NaOH là min hay max nên có 2 trường hợp xảy ra:
Trường hợp 1: Chỉ tạo kết tủa và Al3+ còn dư, khi đó chỉ xảy ra phản ứng tạo kết tủa.
Al3+ + 3OH- → Al(OH)3
0,06 → 0,02
=> [NaOH] = 0,12M.
- TH2: Kết tủa sinh ra và bị hòa tan một phần.
n↓còn lại = 4nAl3+ - nOH- → nOH- = 4nAl3+ - n↓ = 4.0,12 – 0,02 = 0,46 mol.
=> [NaOH] = 0,92M.
Câu 24. Cho lá nhôm vào dung dịch HCl. Lấy dung dịch thu được nhỏ vào vài giọt dung dịch NaOH, hiện tượng xảy ra là:
A. Khí bay lên, xuất hiện kết tủa trắng
B. Có kết tủa trắng xuất hiện
C. Có khí bay lên
D. Không có hiện tượng gì
Lời giải:
Cho lá nhôm vào dung dịch HCl có khí bay lên
2Al + 6HCl → 2AlCl3 + 3H2
Nhỏ từ từ cho đến dư dung dịch NaOH vào dung dịch AlCl3, ban đầu có kết tủa keo trắng xuất hiện.
3NaOH + AlCl3 → Al(OH)3 ↓ + 3NaCl
Câu 25. Có hỗn hợp bột A gồm Al, Fe2O3, Fe3O4 (có cùng số mol). Đem nung 41,9 gam hỗn hợp A ở nhiệt độ cao trong điều kiện không có không khí thu được hỗn hợp B. Hòa tan B trong dung dịch H2SO4 đặc, nóng, dư thu được V lít khí SO2 (là sản phẩm khử duy nhất ở đktc). Giá trị của V là
A. 5,60 lít
B. 11,20 lít
C. 4,48 lít
D. 8,96 lít
Lời giải:
Coi B là hỗn hợp ban đầu
Gọi n(Al) = n(Fe2O3) = n(Fe3O4) = a → 27a + 160a + 232a = 41,9 → a = 0,1 mol
Al0 → Al+3 + 3e S+6 + 2e → S+4
0,1 → 0,3
Fe+8/3 → 3Fe+3 + 1e
0,1 → 0,1
→ n(SO2) = 0,3+0,12 = 0,2 → V = 4,48 lít
Xem thêm các phương trình hóa học liên quan khác:
Al + HNO3 → Al(NO3)3 + N2 + H2O | Al ra Al(NO3)3
Al + HNO3 → Al(NO3)3 + N2O + H2O | Al ra Al(NO3)3
Al + HNO3 → H2O + NO2 + Al(NO3)3 | Al ra Al(NO3)3