Bài tập về Ancol
Kiến thức cần nhớ
Định nghĩa – phân loại
1. Định nghĩa
- Ancol là những hợp chất hữu cơ, trong phân tử có nhóm hiđroxyl – OH liên kết trực tiếp với nguyên tử cacbon no.
- Nhóm OH này được gọi là nhóm – OH ancol.
- Ví dụ một số ancol:
CH3CH2OH; CH2 = CH – CH2 – OH; C6H5 – CH2 – OH.
- Công thức tổng quát của ancol: R(OH)n (n ≥ 1), với R là gốc hiđrocacbon.
- Công thức của ancol no, mạch thẳng, đơn chức: CnH2n+1OH hay CnH2n+2O (với n ≥ 1).
2. Phân loại
- Dựa vào đặc điểm gốc hiđrocacbon, các ancol được chia thành:
+ Ancol no. Ví dụ: CH3OH; CH2OH – CH2OH …
+ Ancol không no. Ví dụ: CH2 = CH – CH2 – OH …
+ Ancol thơm (phân tử có vòng benzen). Ví dụ: C6H5 – CH2 – OH…
- Dựa vào số nhóm OH trong phân tử, ancol được chia thành:
+ Ancol đơn chức: CH3OH; CH2 = CH – CH2 – OH …
+ Ancol đa chức: CH2OH – CH2OH; CH2OH – CH(OH) – CH2OH …
- Các ancol còn được phân loại theo bậc ancol. Bậc của ancol được xác định bằng bậc của nguyên tử C liên kết với nhóm -OH.
Đồng phân, danh pháp
1. Đồng phân
Các ancol no, mạch hở, đơn chức có đồng phân mạch cacbon và đồng phân vị trí nhóm chức – OH trong mạch cacbon.
Ví dụ: C4H10O có các đồng phân ancol như sau:
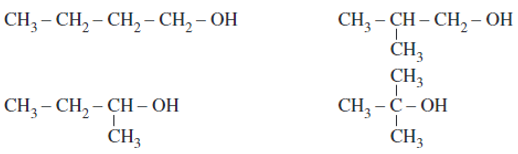
2. Danh pháp
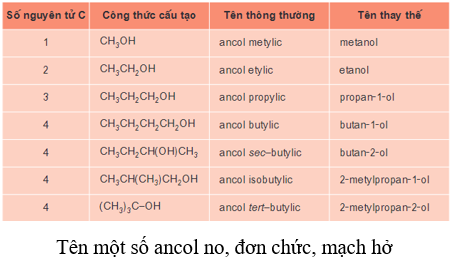
a) Tên thông thường
- Một số ít ancol có tên thông thường.
- Tên thông thường = Ancol + tên gốc ankyl+ ic.
Ví dụ:
CH3-CH2-OH: ancol etylic.
CH3-OH: ancol metylic.
b) Tên thay thế
Các bước gọi tên thay thế:
-Chọn mạch chính của phân tử ancol là mạch dài nhất có chứa nhóm -OH.
- Đánh số thứ tự nguyên tử cacbon trên mạch chính bắt đầu từ phía gần nhóm -OH hơn.
- Tên thay thế = tên hiđrocacbon tương ứng với mạch chính + số chỉ vị trí nhóm OH + ol.
- Ví dụ:
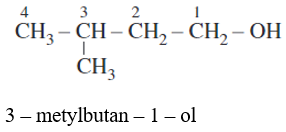
Tính chất vật lý
- Các ancol là chất lỏng hoặc chất rắn ở điều kiện thường.
- Nhiệt độ sôi, khối lượng riêng của các ancol tăng theo chiều tăng của phân tử khối, ngược lại độ tan trong nước của chúng lại giảm khi phân tử khối tăng.
- Các ancol có nhiệt độ sôi cao hơn các hiđcacbon có cùng phân tử khối hoặc đồng phân ete của nó là do giữa các phân tử ancol có liên kết hiđro ⇒ Ảnh hưởng đến độ tan.
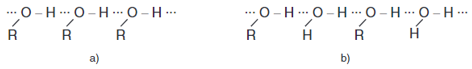
Liên kết hiđro giữa các phân tử ancol với nhau (a) và với nước (b)
Tính chất hóa học
Trong phân tử ancol liên kết C – OH, đặc biệt liên kết O – H phân cực mạnh nên nhóm – OH nhất là nguyên tử H dễ bị thay thế hoặc tách ra trong các phản ứng hóa học.
1. Phản ứng thế H của nhóm OH ancol (phản ứng đặc trưng của ancol)
- Tính chất chung của ancol tác dụng với kim loại kiềm:
Ví dụ:
2CH3CH2OH + 2Na → 2CH3CH2ONa + H2
Tổng quát:
+ Với ancol đơn chức:
2ROH + 2Na → 2RONa + H2↑
+ Với ancol đa chức:
2R(OH)x + 2xNa → 2R(ONa)x + xH2↑
- Tính chất đặc trưng của glixerol hòa tan Cu(OH)2
Ví dụ:
2C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + 2H2O
Không chỉ glixerol, các ancol đa chức có các nhóm – OH liền kề cũng có tính chất này.
⇒ Phản ứng này dùng để phân biệt ancol đơn chức với ancol đa chức có các nhóm - OH cạnh nhau trong phân tử.
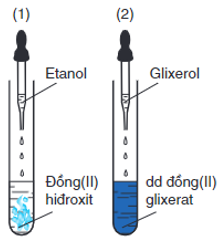
Thí nghiệm về phản ứng đặc trưng của glixerol
2. Phản ứng thế nhóm OH
a) Phản ứng với axit vô cơ:
Ví dụ:
C2H5OH + HBr C2H5Br + H2O
Các ancol khác cũng có phản ứng tương tự, phản ứng này chứng tỏ phân tử ancol có nhóm – OH.
b) Phản ứng với ancol
Ví dụ:
2C2H5OH C2H5OC2H5 + H2O
C2H5OC2H5: đietyl ete
⇒ Công thức tính số ete tạo thành từ n ancol khác nhau là
3. Phản ứng tách nước (phản ứng đehidrat hoá)
Ví dụ:
CH3CH2OH CH2 = CH2 + H2O
Trong điều kiện tương tự, các ancol no, đơn chức, mạch hở (trừ CH3OH) có thể bị tách nước tạo thành anken. Tổng quát:
CnH2n + 1OH CnH2n + H2O
4. Phản ứng oxi hoá
- Phản ứng oxi hoá hoàn toàn:
Khi bị đốt các ancol cháy, tỏa nhiều nhiệt. Tổng quát cho đốt cháy ancol no, đơn chức, mạch hở:
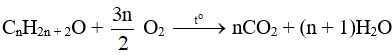
- Phản ứng oxi hoá không hoàn toàn bởi CuO, to
+ Các ancol bậc I bị oxi hóa không hoàn toàn tạo thành anđehit. Ví dụ:
CH3CH2OH + CuO CH3CHO (anđehit axetic) + Cu + H2O
+ Các ancol bậc II bị oxi hóa không hoàn toàn tạo thành xeton. Ví dụ:
CH3- CH(OH) – CH3 + CuO CH3 – CO – CH3 + Cu + H2O
+ Trong điều kiện trên, ancol bậc III không phản ứng.
Điều chế
a. Phương pháp tổng hợp
Anken + H2O ancol
Ví dụ:
CH2 = CH2 + H2O CH3 – CH2 – OH
b. Phương pháp sinh hoá: từ tinh bột, đường, ... lên men.
(C6H10O5)n C6H12O6 C2H5OH
VI. Ứng dụng
Etanol có nhiều ứng dụng trong nhiều lĩnh vực, thể hiện trong hình dưới đây:

Các dạng bài tập về ancol
Dạng 1: Cấu tạo, đồng phân, danh pháp, tính chất vật lí, ứng dụng
Dạng 2: Phản ứng hoá học, nhận biết, điều chế
Dạng 3: Bài toán định lượng và xác định công thức phân tử, công thức cấu tạo của ancol trong dãy đồng đẳng
Bài tập tự luyện
1. Bài tập vận dụng
Câu 1: Cả phenol và ancol etylic đều phản ứng được với
A. Na
B. NaOH
C. Br2
D. NaHCO3.
Câu 2: Phát biểu nào sau đây không đúng ?
A. Dung dịch natri phenolat phản ứng với khí CO2 lấy chất hữu cơ vừa tạo ra cho tác dụng với dung dịch NaOH lại thu được natri phenolat.
B. Phenol phản ứng với dung dịch NaOH, lấy muối vừa tạo ra cho tác dụng với dung dịch HCl lại thu được phenol.
C. Cho ancol etylic tác dụng với Na lấy chất rắn thu được hòa tan vào nước lại thu được ancol etylic.
D. Cho ancol metylic đi qua H2SO4 đặc ở 170oC tạo thành ankan.
Câu 3: Cho các chất : ancol etylic, glixerol, etylen glicol, dimetyl ete và propan-1-3-điol. Số chất tác dụng được với Cu(OH)2 là
A. 1
B. 3
C. 4
D. 2
Câu 4: Ancol nào sau đây phản ứng với CuO không tạo thành anđehit ?
A. metanol.
B. etanol
C. 2-metylpropanol-1.
D. propanol-2.
Câu 5: đun nóng hỗn hợp gồm hai ancol đơn chức, mạch hở, kế tiếp nhau trong dãy đồng đẳng với H2SO4 đặc ở 140oC. Sau khi các phản ứng kết thúc , thu được 6 gam hỗn hợp gồm ba ete và 1,8 gam nước. Công thức phân tử của hai rượu trên là
A. CH3OH và C2H5OH .
B. C2H5OH và C3H7OH
C. C3H5OH và C4H2OH.
D. C3H7OH và C4H9OH .
Câu 6: Đung nóng một ancol đơn chức X với dung dịch H2SO4 đăc trong điều kiện nhiệt độ thích hợp sinh ra chất hữu cơ Y, tỉ khối hơi của X so với Y là 0,6956. Công thức phân tử của Y là
A. C3H8O.
B. C2H6O
C. CH4O.
D. C4H8O .
Câu 7: Khi đốt cháy hoàn toàn m gam hỗn hợp hai ancol no đơn chức, mạch hở thu được V lít khí CO2 (đktc) và a gam H2O. Biểu thức liên hệ giữa m, a vầ V là
A. m = 2a – V/22,4 .
B. m = 2a – V/11,2
C. m = a + V/5,6.
D. m = a – V/5,6 .
Câu 8: Đốt cháy hoàn toàn a gam C2H5OH thu được 0,2 mol CO2. Đốt cháy hoàn toàn b gam CH3COOH thu được 0,2 mol CO2. Cho a gam C2H5OH tác dụng với b gam CH3COOH có xúc tác là H2SO4 đặc và đun nóng ( giả sử hiệu suất phản ứng là 100%) thì thu được số gam ete là
A. 8,8 gam .
B. 17,6 gam
C. 4,4 gam.
D. 13,2 gam.
Câu 9: Cho Na tác dụng vừa đủ với 1,24 gam hỗn hợp 3 ancol đơn chức X, Y, Z thấy thoát ra 0,336 lít khí H2 (đkc). Khối lượng muối natri ancolat thu được là
A. 2,4 gam
B. 1,9 gam.
C. 2,85 gam.
D. 3,8 gam.
Câu 10: Lên men dung dịch chứa 300 gam glucozơ thu được 92 gam ancol etylic. Hiệu suất của quá trình lên men tạo thành ancol etylic là:
A. 40%
B. 60%
C. 54%
D. 80%
Câu 11: Một loại rượu có khối lượng riêng D = 0,92 g/ml thì độ rượu là bao nhiêu ? Biết khối lượng riêng của H2O và C2H5OH lần lượt là 1 và 0,8 g/ml (bỏ qua sự co dãn thể tích sau khi trộn)
A. 45o
B. 39,5o
C. 90o
D. 40o
Câu 12: Cho 2 phản ứng:
(1) 2CH3COOH + Na2CO3 → 2CH3COONa + H2O + CO2
(2) C6H5ONa + CO2 + H2O → C6H5OH + NaHCO3
Hai phản ứng trên chứng tỏ lực axit theo thứ tự CH3COOH, H2CO3, C6H5OH, HCO3- là
A. Tăng dần.
B. Giảm dần.
C. Không thay đổi.
D. Vừa tăng vừa giảm.
Câu 13: Dãy gồm các chất đều phản ứng với phenol là:
A. dung dịch NaCl, dung dịch NaOH, kim loại Na.
B. nước brom, axit axetic, dung dịch NaOH.
C. nước brom, anhiđrit axetic, dung dịch NaOH.
D. nước brom, anđehit axetic, dung dịch NaOH.
Câu 14: Một hỗn hợp gồm 25 gam phenol và benzen khi cho tác dụng với dung dịch NaOH dư thấy tách ra 2 lớp chất lỏng phân cách, lớp chất lỏng phía trên có thể tích 19,5 ml và có khối lượng riêng là 0,8 g/ml. Khối lượng phenol trong hỗn hợp ban đầu là :
A. 15,6 gam
B. 9,4 gam
C. 24,375 gam
D. 0,625 gam
Câu 15: Cho 18,8 gam phenol tác dụng với 45g dung dịch HNO3 63% (có H2SO4 làm xúc tác ). Hiệu suất phản ứng là 100%. Khối lượng axit picric thu được là
A. 50g
B. 34,35g
C. 34,55g
D. 35g
Đáp án và lời giải chi tiết bộ 15 câu hỏi trắc nghiệm Hóa 11 Bài 41: Ancol và phenol
Câu 1:
Đáp án: A
Câu 2:
Đáp án: D
Câu 3:
Đáp án: D
Câu 4:
Đáp án: D
Câu 5:
Đáp án: A
2R-OH → R2O + H2O
Áp dụng định luật bảo toàn khối lượng
mancol = mete + mH2O = 7,8g
nancol = 2nH2O = 0,2 mol ⇒ Mancol = 7,8 : 0,2 = 39 ⇒ R = 22 ⇒ -CH3 (15) và –C2H5 (29)
⇒ CH3OH và C2H5OH
Câu 6:
Đáp án: C
dX/Y < 1 ⇒ Y là ete
Ta có MY = 2MX - 18
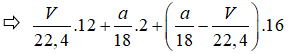
⇒ MX = 32 ⇒ X là CH4O
Câu 7:
Đáp án: D
ancol no đơn chức mạch hở ⇒ nO (ancol) = nancol = nH2O – nCO2 = a/18 - V/22,4
m = mC + mH + mO = 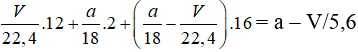
Câu 8:
Đáp án: A
nC2H5OH = 1/2 nCO2 = 0,1 mol; nCH3COOH = 0,1 mol
CH3COOH + C2H5OH ⇌ CH3COOC2H5 + H2O
meste = 0,1.88 = 8,8 (gam)
Câu 9:
Đáp án: B
ROH + Na → RONa + 1/2 H2
nNa = 2nH2 = 0,03 mol
Áp dụng định luật bảo toàn khối lượng:
mMuối = ancol + mNa - H2 = 1,24 + 0,03.23 – 0,015.2 = 1,9g
Câu 10:
Đáp án: B
C6H12O6 → 2C2H5OH
180g 92g
300g → 153,3g
H% = (92/153,3). 100% = 60%
Câu 11:
Đáp án: D
Giả sử có 100ml dung dịch rượu có x ml C2H5OH nguyên chất và y ml nước → x + y = 100
Khối lượng của 100 ml dung dịch rượu là 0,8x + y
Khối lượng riêng của dung dịch rượu là → (0,8x + y)/100 = 0,92 → 0,8x + y = 92
Giải hệ ⇒ x = 40 , y = 60
Vậy độ rượu của dung dịch là 40o
Câu 12:
Đáp án: B
Câu 13:
Đáp án: C
Câu 14:
Đáp án: B
Lớp chất lỏng phía trên có V = 19,5ml ⇒ Vbenzen = 19,5 ( Do benzen không tác dụng với dung dịch NaOH, không tan trong H2O)
mbenzen = V.D = 15,6g ⇒ mphenol = 9,4g
Câu 15:
Đáp án: B
nphenol = 0,2 mol; nHNO3 = 0,45 mol
C6H5OH + 3HNO3 → C6H2(NO2)3OH + 3H2O
⇒ HNO3 hết; npicric = 1/3 nHNO3 = 0,15 mol
⇒ mpicric = 0,15. 229 = 34,35g
2. Bài tập tự luyện có hướng dẫn
(Xem thêm trong file dưới)
Xem thêm các dạng bài tập và câu hỏi liên quan khác
500 Bài tập Hóa 11 Chương 6: Hiđrocacbon không no (có đáp án)
500 Bài tập Hóa 11 Chương 5: Hiđrocacbon no (có đáp án)
500 Bài tập Hóa 11 Chương 3: Cacbon - Silic (có đáp án)
500 Bài tập Hóa 11 Chương 2: Nitơ - Photpho (có đáp án)
70 Bài tập Axit cacboxylic (có đáp án)