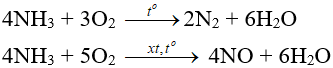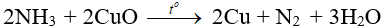Phương trình điện li NH3
1. Viết phương trình điện li của NH3
NH3+ H2O ⇆ NH4+ + OH−
2. NH3 là chất điện li yếu
NH3 là bazơ còn H2O là axit, ngược lại NH4+ là axit còn OH- là bazơ.
NH3 là chất điện li yếu và là bazơ yếu.
3. Tính chất hóa học của NH3
3.1. Tính bazơ yếu
- Tác dụng với nước:
NH3 + H2O ⇋ NH4+ + OH-
⇒ Dung dịch NH3 là một dung dịch bazơ yếu.
- Tác dụng với dung dịch muối (muối của những kim loại có hidroxit không tan):
AlCl3 + 3NH3 + 3H2O → Al(OH)3↓ + 3NH4Cl
Al3+ + 3NH3 + 3H2O → Al(OH)3↓ + 3NH4+
- Tác dụng với axit → muối amoni:
NH3 + HCl → NH4Cl (amoni clorua)
2NH3 + H2SO4 → (NH4)2SO4 (amoni sunfat)
3.2. Khả năng tạo phức
Dung dịch amoniac có khả năng hòa tan hiđroxit hay muối ít tan của một số kim loại, tạo thành các dung dịch phức chất.
Ví dụ:
* Với Cu(OH)2:
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2 (màu xanh thẫm)
* Với AgCl:
AgCl + 2NH3 → [Ag(NH3)2]Cl
Sự tạo thành các ion phức là do sự kết hợp các phân tử NH3 bằng các electron chưa sử dụng của nguyên tử nitơ với ion kim loại.
3.3. Tính khử
- Amoniac có tính khử: phản ứng được với oxi, clo và khử một số oxit kim loại (Nitơ có số oxi hóa từ -3 đến 0, +2).
- Tác dụng với oxi:
- Tác dụng với clo:
2NH3 + 3Cl2 → N2 + 6HCl
NH3 kết hợp ngay với HCl vừa sinh ra tạo “khói trắng” NH4Cl
- Tác dụng với CuO:
4. Bài tập vận dụng liên quan
Câu 1. Cho các chất dưới đây: H2O, HCl, NaOH, KCl, CH3COOH, CuSO4, HF, Al(OH)3. Các chất điện li yếu là:
A. H2O, KCl, CH3COOH, Al(OH)3
B. Al(OH)3, CH3COOH, H2O, NaOH.
C. H2O, CH3COOH, Al(OH)3, HF
D. H2O, CH3COOH, CuSO4, HgF
Lời giải:
Câu 2. Phương trình hóa học nào sau đây không đúng?
A. ZnS + 2HCl → ZnCl2 + H2S
B. FeCl2 + H2S → FeS + 2HCl
C. 2FeCl3 + H2S → 2FeCl2 + S↓ + 2HCl
D. 4FeS2 + 11O2 → 2Fe2O3 + 8SO2↑
Lời giải:
Câu 3. Hidroxit nào sau đây không phải là hidroxit lưỡng tính?
A. Pb(OH)2
B. Al(OH)3
C. Ba(OH)2
D. Zn(OH)2
Lời giải:
Câu 4. Hòa tan m gam Na vào nước được 100 ml dung dịch có pH = 13. Giá trị của m bằng
A. 0,23.
B. 2,3.
C. 3,45.
D. 0,46.
Lời giải: