Trắc nghiệm KHTN 7 Bài 7: Hóa trị và công thức hóa học (Phần 2) có đáp án
Trắc nghiệm KHTN 7 Bài 7: Hóa trị và công thức hóa học (Phần 2) có đáp án
-
61 lượt thi
-
10 câu hỏi
-
0 phút
Danh sách câu hỏi
Câu 1:
Cho hình mô phỏng phân tử ammonia:
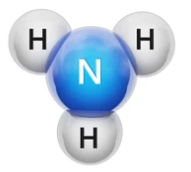
Hóa trị của nguyên tố nitrogen trong phân tử ammonia là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Để xác định hóa trị của nguyên tố trong hợp chất cộng hóa trị, người ta dựa vào hóa trị của nguyên tố đã biết làm đơn vị, chẳng hạn hóa trị của H là I, hóa trị của O là II.
Trong phân tử ammonia, nguyên tử N liên kết với 3 nguyên tử H (mỗi nguyên tử H hóa trị I) nên hóa trị của nguyên tử N là III.
Câu 2:
Cho hình mô phỏng phân tử silicon dioxide:
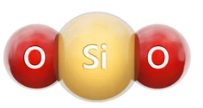
Trong tự nhiên, silicon dioxide có nhiều trong cát, đất sét, ... Hóa trị của nguyên tố silicon trong phân tử silicon dioxide là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Để xác định hóa trị của nguyên tố trong hợp chất cộng hóa trị, người ta dựa vào hóa trị của nguyên tố đã biết làm đơn vị, chẳng hạn hóa trị của H là I, hóa trị của O là II.
Trong phân tử silicon dioxide, nguyên tử Si liên kết với 2 nguyên tử O (mỗi nguyên tử O hóa trị II) nên hóa trị của nguyên tử Si là IV.
Câu 3:
Phân tử khí ozone được tạo thành từ 3 nguyên tử ozone liên kết với nhau. Công thức hóa học của phân tử khí ozone là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Công thức hóa học dùng để biểu diễn chất, gồm một hoặc nhiều kí hiệu nguyên tố và chỉ số ở bên dưới mỗi kí hiệu.
Công thức hóa học của phân tử khí ozone là O3.
Câu 4:
Phân tử methane gồm một nguyên tử carbon liên kết với 4 nguyên tử oxygen. Công thức hóa học của phân tử methane là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Công thức hóa học dùng để biểu diễn chất, gồm một hoặc nhiều kí hiệu nguyên tố và chỉ số ở bên dưới mỗi kí hiệu.
Công thức hóa học của phân tử methane là CH4.
Câu 5:
Công thức hóa học của iron(III) oxide là Fe2O3. Nhận định nào sau đây là sai?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Iron(III) oxide do hai nguyên tố Fe, O tạo ra A đúng
Trong một phân tử iron(III) oxide có hai nguyên tử Fe, ba nguyên tử O B đúng
Khối lượng phân tử iron(III) oxide là:
2.56 + 3.16 = 160 amu C đúng
Trong phân tử iron(III) oxide tỉ lệ số nguyên tử Fe : O là 2 : 3 D sai
Câu 6:
Một hợp chất có công thức NxOy, trong đó N chiếm 30,43%. Khối lượng phân tử hợp chất là 46 amu. Công thức hóa học của hợp chất là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Ta có %O = 100% - %N = 100% - 30,43% = 69,57%.
%N = \[\frac{{KLNT(N) \times x}}{{KLPT({N_x}{O_y})}}\]×100% = \[\frac{{14 \times x}}{{46}}\]×100% = 30,43%
x = 1
%O = \[\frac{{KLNT(O) \times y}}{{KLPT({N_x}{O_y})}}\]×100% = \[\frac{{16 \times y}}{{46}}\]×100% = 69,57%
x = 2
Công thức hóa học của hợp chất là NO2.
Câu 7:
Soda là hóa chất được dùng rộng rãi trong các ngành công nghiệp thủy tinh, đồ gốm, xà phòng, phẩm nhuộm. Xác định công thức hóa học của soda biết soda có cấu tạo từ Na hóa trị I và nhóm CO3 hóa trị II?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Gọi công thức chung của soda là \(Na_x^I(C{O_3})_y^{II}\).
Áp dụng quy tắc hóa trị:
x.I = y.II → \(\frac{x}{y}\)= \(\frac{{II}}{I}\)= \(\frac{2}{1}\)
Lấy x = 2 và y = 1.
Công thức hóa học của soda là Na2CO3.
Câu 8:
Pháo hoa có thành phần nhiên liệu nổ gồm sulfur, than và potassium nitrate. Biết potassium nitrate có công thức hóa học là KNO3. Thành phần phần trăm khối lượng của các nguyên tố K, N và O trong potassium nitrate lần lượt là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Khối lượng phân tử KNO3 là:
1.39 + 1.14 + 3.16 = 101 (amu)
Phần trăm khối lượng của các nguyên tố trong KNO3 là:
%K = \(\frac{{1.39.100\% }}{{101}}\)= 38,61%
%N = \(\frac{{1.14.100\% }}{{101}}\)= 13,86%
%O = 100% - %K - %N = 100% - 38,61% - 13,86% = 47,53%
Câu 9:
Bột thạch cao có nhiều ứng dụng quan trọng trong đời sống. Thành phần chính của bột thạch cao là hợp chất A. Phân tử A có cấu tạo từ nguyên tố calcium (Ca), sulfur (S) và oxygen (O) với tỉ lệ phần trăm tương ứng là 29,41%, 23,53% và 47,06%. Biết khối lượng phân tử của A là 136 amu, công thức hóa học của A là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Gọi công thức hóa học của hợp chất A là CaxSyOz.
Phần trăm khối lượng của các nguyên tố trong hợp chất là:
%Ca = \[\frac{{KLNT(Ca) \times x}}{{KLPT(A)}}\]×100% = \[\frac{{40 \times x}}{{136}}\]×100% = 29,41%
x = 1
%S = \[\frac{{KLNT(S) \times y}}{{KLPT(A)}}\]×100% = \[\frac{{32 \times y}}{{136}}\]×100% = 23,53%
y = 1
%O = \[\frac{{KLNT(O) \times z}}{{KLPT(A)}}\]×100% = \[\frac{{16 \times z}}{{136}}\]×100% = 47,06%
z = 4
Vậy công thức hóa học của hợp chất A là CaSO4.
Câu 10:
Thạch nhũ trong hang động có thành phần chính là hợp chất T. Phân tử T có cấu tạo từ nguyên tố calcium, carbon và oxygen với tỉ lệ phần trăm tương ứng là 40%, 12% và 48%. Khối lượng phân tử của T là 100 amu. Nhận định nào sau đây là sai?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Gọi công thức hóa học của hợp chất T là CaxCyOz.
Phần trăm khối lượng của các nguyên tố trong hợp chất là:
%Ca = \[\frac{{KLNT(Ca) \times x}}{{KLPT(T)}}\]×100% = \[\frac{{40 \times x}}{{100}}\]×100% = 40%
x = 1
%S = \[\frac{{KLNT(C) \times y}}{{KLPT(T)}}\]×100% = \[\frac{{12 \times y}}{{100}}\]×100% = 12%
y = 1
%O = \[\frac{{KLNT(O) \times z}}{{KLPT(T)}}\]×100% = \[\frac{{16 \times z}}{{100}}\]×100% = 48%
z = 3
Vậy công thức hóa học của hợp chất T là CaCO3 C đúng
Trong một phân tử T có 1 nguyên tử Ca, 1 nguyên tử C và 3 nguyên tử O B sai.
Trong hai phân tử T có 2 nguyên tử Ca, 2 nguyên tử C và 6 nguyên tử O D đúng.
Trong phân tử T tỉ lệ số nguyên tử Ca: C: O là 1 : 1 : 3 A đúng.
