Trắc nghiệm Hóa học 10 Bài 7. Định luật tuần hoàn -Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học có đáp án
Trắc nghiệm Hóa học 10 Bài 7. Định luật tuần hoàn -Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học có đáp án
-
96 lượt thi
-
15 câu hỏi
-
0 phút
Danh sách câu hỏi
Câu 1:
Phát biểu đúng về định luật tuần hoàn là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Phát biểu đúng về định luật tuần hoàn là:
Tính chất của các nguyên tố và đơn chất, cũng như thành phần và tính chất của hợp chất tạo nên từ các nguyên tố đó biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân nguyên tử.
Câu 2:
Nguyên tử nguyên tố G có cấu hình electron là [Ne] 3s23p4. Vị trí của G trong bảng tuần hoàn là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
G có cấu hình electron: [Ne] 3s23p4⇒ Z = 16
G có Z = 16 ⇒ G ở ô thứ 16;
G có 3 lớp electron ⇒ G ở chu kì 3;
G là nguyên tố p, có 6 electron lớp ngoài cùng ⇒ G ở nhóm VIA
Câu 3:
Nguyên tử nguyên tố X có cấu hình e là [Ar] 3d64s2. Vị trí của X trong bảng tuần hoàn là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
X có cấu hình electron: [Ar] 3d64s2
X có 4 lớp electron ⇒ X ở chu kì 4;
X là nguyên tố d, có 8 electron hóa trị (electron lớp ngoài cùng và phân lớp sát lớp ngoài cùng chưa bão hòa) ⇒ X ở nhóm VIIIB.
Câu 4:
Các nguyên tố trong bảng tuần hoàn được sắp xếp theo chiều tăng dần
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Các nguyên tố trong bảng tuần hoàn được sắp xếp theo chiều tăng dần số hiệu nguyên tử.
Câu 5:
Nguyên tố Ca có số hiệu nguyên tử là 20. Phát biểu nào sau đây về Ca là không đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Nguyên tố Ca có số hiệu nguyên tử là 20 ⇒ số electron = số proton = Z = 20 ⇒ A, C đúng.
Z = 20 ⇒ Cấu hình electron nguyên tử là: [Ar]4s2⇒ có 4 lớp electron và lớp ngoài cùng có 2 electron ⇒ B đúng.
Có 2 electron lớp ngoài cùng ⇒ nguyên tố kim loại. ⇒ D sai.
Câu 6:
Nguyên tố Y ở chu kì 3, nhóm IA trong bảng tuần hoàn. Tính chất hóa học cơ bản của Y là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Y ở chu kì 3, nhóm IA trong BTH ⇒ Y là kim loại mạnh.
Câu 7:
Y thuộc chu kì 4, nhóm IIA. Công thức oxide và hydroxide cao nhất của Y lần lượt là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Hóa trị cao nhất của các nguyên tố thuộc nhóm IA đến VIIA (trừ F) = số thứ tự của nhóm.
Y thuộc chu kì 4, nhóm IIA ⇒ Y là kim loại và hóa trị cao nhất của Y là II
Công thức oxide cao nhất là: YO
Công thức hydroxide cao nhất là Y(OH)2
Câu 8:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Nguyên tố potassium thuộc ô 19 trong bảng tuần hoàn
⇒ số hiệu nguyên tử Z = số thứ tự của ô nguyên tố = 19.
Z = 19 ⇒ có 19 electron.
Do đó cấu hình electron là: [Ar]4s1
⇒ Có 4 lớp electron và lớp ngoài cùng có 1 electron.
Vậy khẳng định A là khẳng định đúng.
Câu 9:
Nguyên tử nguyên tố sulfur (S) có 16 proton. Công thức oxide cao nhất và tính chất của oxide đó là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Nguyên tử nguyên tố sulfur (S) có 16 proton ⇒ Z = 16
Cấu hình electron của S: [Ne]3s23p4⇒ chu kì 3, nhóm VIA
Hóa trị cao nhất của S = số thứ tự nhóm A = VI ⇒ Công thức oxide cao nhất là: SO3
S có 6 electron lớp ngoài cùng ⇒ S là nguyên tố phi kim ⇒ Oxide có tính acid oxide.
Câu 10:
Nguyên tố chlorine ở chu kì 3, nhóm VIIA trong bảng tuần hoàn. Cấu hình electron nguyên tử của chlorine là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Nguyên tố chlorine ở chu kì 3 ⇒ có 3 lớp electron và lớp ngoài cùng là lớp thứ 3.
Nhóm VIIA ⇒ nguyên tố p và có 7 electron lớp ngoài cùng ⇒ Cấu hình electron lớp ngoài cùng là: 3s23p5.
⇒ Cấu hình electron: [Ne]3s23p5
Câu 11:
Cho 4 gam oxide của kim loại X (thuộc nhóm IIA) tác dụng vừa đủ với 200 ml dung dịch HCl 1M. Kim loại X là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
X thuộc nhóm IIA ⇒ hóa trị II ⇒ Công thức oxide có dạng: XO
nHCl= 0,2.1 = 0,2 (mol)
XO + 2HCl ⟶ XCl2+ H2O
0,1 ← 0,2 (mol)
MXO= 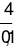 = 40 (g/mol)
= 40 (g/mol)
Mà MXO= MX+ 16 ⇒ MX+ 16 = 40 ⇒ MX= 24 (g/mol)
Vậy X là Mg
Câu 12:
Cho X (Z = 9), Y (Z = 17) và T (Z = 16). Sắp xếp các nguyên tố theo thứ tự bán kính nguyên tử tăng dần.
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Cấu hình electron của X (Z = 9): 1s22s22p5⇒ chu kì 2, nhóm VIIA
Cấu hình electron của Y (Z = 17): [Ar]3s23p5⇒ chu kì 3, nhóm VIIA
Cấu hình electron của T (Z = 16): [Ar]3s23p4⇒ chu kì 3, nhóm VIA
Y và T cùng thuộc chu kì 3 mà điện tích hạt nhân của T < Y.
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân bán kính nguyên tử có xu hướng giảm.
Do đó, bán kính nguyên tử của T >Y
X và Y cùng thuộc nhóm VIIA mà điện tích hạt nhân của X < Y.
Trong cùng một nhóm, theo chiều tăng dần của điện tích hạt nhân bán kính nguyên tử có xu hướng tăng.
Do đó, bán kính nguyên tử của X < Y
Vậy bán kính nguyên tử của X < Y < T.
</></></></>
Câu 13:
Oxide cao nhất của X khi tan trong nước tạo thành dung dịch làm quỳ tím chuyển màu xanh. Tỉ lệ nguyên tử X với oxygen trong oxide cao nhất của X là 2 : 1. X thuộc nhóm
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Oxide cao nhất của X khi tan trong nước tạo thành dung dịch làm quỳ tím chuyển màu xanh. ⇒ Oxide cao nhất của X khi tan trong nước tạo thành hydroxide có tính base mạnh. ⇒ X có thể thuộc nhóm IA hoặc IIA.
Tỉ lệ nguyên tử X với oxygen trong oxide cao nhất của X là 2 : 1 ⇒ Oxide cao nhất của X là X2O ⇒ Hóa trị cao nhất của X là I.
Vậy X thuộc nhóm IA.
Câu 14:
Hydroxide của nguyên tố T có tính base mạnh và tác dụng được với dung dịch H2SO4theo tỉ lệ mol giữa hydroxide của T và HCl là 1 : 1. Nhóm của T trong bảng tuần hoàn là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Hydroxide của nguyên tố T có tính base mạnh ⇒ công thức có dạng: T(OH)x
2T(OH)x+ xH2SO4⟶ T2(SO4)x+ 2xH2O
Mà tỉ lệ mol giữa hydroxide của T và H2SO4là 1 : 1 ⇒ x = 2
⇒ T có hóa trị II mà hydroxide của T có tính base mạnh ⇒ T thuộc nhóm IIA
Câu 15:
Y là nguyên tố nhóm A có công thức oxide cao nhất là Y2O5. Y thuộc nhóm
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Công thức oxide cao nhất của Y là Y2O5⇒ Hóa trị cao nhất của Y là V
Y là nguyên tố nhóm A nên số thứ tự nhóm = hóa trị cao nhất = V
Vậy Y thuộc nhóm VA.
