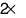Trắc nghiệm Hóa học 10 Bài 12. Phản ứng oxi hóa - khử và ứng dụng trong cuộc sống có đáp án
Trắc nghiệm Hóa học 10 Bài 12. Phản ứng oxi hóa - khử và ứng dụng trong cuộc sống có đáp án
-
142 lượt thi
-
15 câu hỏi
-
0 phút
Danh sách câu hỏi
Câu 1:
Số oxi hóa của một nguyên tử trong phân tử được định nghĩa là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Số oxi hóa của một nguyên tử trong phân tử là điện tích của nguyên tử nguyên tố đó nếu giả định cặp electron chung thuộc hẳn về nguyên tử của nguyên tố có độ âm điện lớn hơn.
Câu 2:
Cho nguyên tố X có số oxi hóa có giá trị là -2. Cách biểu diễn đúng là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Cách biểu diễn số oxi hóa:
+ Số oxi hóa được đặt ở phía trên kí hiệu nguyên tố.
+ Dấu điện tích được đặt ở phía trước, số ở phía sau.
Do đó, nguyên tố X có số oxi hóa có giá trị là âm 2 được biểu diễn là: 
Câu 3:
Số oxi hóa của các nguyên tử trong H2, Fe2+, Cl− lần lượt là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Ta có: số oxi hóa của nguyên tử nguyên tố trong đơn chất bằng 0. Do đó số oxi hóa của H trong H2 là 0.
Trong ion, số oxi hóa của nguyên tử bằng điện tích của ion. Do đó:
Fe2+ có điện tích là 2+ nên Fe có số oxi hóa là +2.
Cl− có điện tích là 1− nên Cl có số oxi hóa là −1.
Câu 4:
Phát biểu nào sau đây sai khi nói về số oxi hóa trong hợp chất?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Trong hợp chất, số oxi hóa của O thường là –2 (trừ một số trường hợp như OF2, H2O2, …)
Vậy phát biểu B là sai.
Câu 5:
Số oxi hóa của Mn trong các phân tử MnO2, KMnO4, K2MnO4 lần lượt là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Gọi số oxi hóa của nguyên tử Mn là x, theo quy tắc 1 và 2 về xác định số oxi hóa, ta có:
Trong phân tử MnO2: 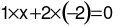 ⇒ x = +4
⇒ x = +4
Trong phân tử KMnO4: 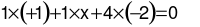 ⇒ x = +7
⇒ x = +7
Trong phân tử K2MnO4: 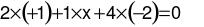 ⇒ x = +6.
⇒ x = +6.
Câu 6:
Số oxi hóa của nguyên tử N trong các ion NH4+, NO3−, NO2− lần lượt là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Gọi số oxi hóa của nguyên tử N là x, theo quy tắc 1 và 2 về xác định số oxi hóa, ta có:
Trong ion NH4+: 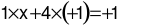 ⇒ x = −3
⇒ x = −3
Trong ion NO3−: 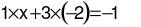 ⇒ x = +5
⇒ x = +5
Trong ion NO2−: 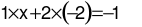 ⇒ x = +3
⇒ x = +3
Câu 7:
Cho phân tử CH4 công thức cấu tạo dưới đây. Số oxi hóa của C là
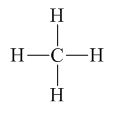
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Trong mỗi liên kết C−H, H góp 1 electron, khi giả định CH4 là hợp chất ion thì electron này chuyển sang C.
Vì có 4 liên kết C −H nên số oxi hóa của C là −4.
Câu 8:
Phát biểu sai là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Phản ứng oxi hóa – khử có thể chỉ có quá trình oxi hóa hoặc quá trình khử là phát biểu sai vì phản ứng oxi hóa – khử luôn xảy ra đồng thời quá trình oxi hóa và quá trình khử.
Câu 9:
Chất khử là chất
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Chất khử là chất nhường electron, có số oxi hóa tăng, bị oxi hóa.
Chất oxi hóa là chất nhận electron, có số oxi hóa giảm, bị khử.
Câu 10:
Phản ứng nào dưới đây là phản ứng oxi hóa – khử?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
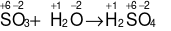
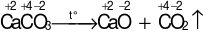
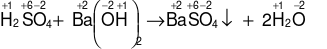
Trong phản ứng không có nguyên tố nào thay đổi số oxi hóa ⇒ không phải phản ứng oxi hóa – khử.
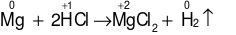
Mg có số oxi hóa tăng từ 0 lên +2; H có số oxi hóa giảm từ +1 về 0. ⇒ Trong phản ứng có 2 nguyên tố thay đổi số oxi hóa. ⇒ Đây là phản ứng oxi hóa – khử.
Câu 11:
Cho phản ứng: Fe + CuSO4 ⟶ Cu + FeSO4.
Khẳng định đúng là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B

Cu2+ (CuSO4) có số oxi hóa giảm sau phản ứng ⇒ Cu2+ đã nhận electron ⇒ Chất oxi hóa là Cu2+
Fe có số oxi hóa tăng sau phản ứng ⇒ Fe đã nhường electron ⇒ Chất khử là Fe.
Câu 12:
Cho phản ứng: 3Cu + 8H+ + 2NO3−⟶3Cu2+ + 2NO + 4H2O
Quá trình khử là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Quá trình khử là quá trình chất oxi hóa nhận electron.
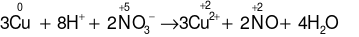
Vậy quá trình khử trong phản ứng: 3Cu + 8H+ + 2NO3−⟶3Cu2+ + 2NO + 4H2O là
 + 3e ⟶
+ 3e ⟶
Câu 13:
Cho phản ứng: 4P + 5O2⟶ 2P2O5
Quá trình oxi hóa là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Quá trình oxi hóa là quá trình chất khử nhường electron.

Vậy quá trình oxi hóa của phản ứng 4P + 5O2⟶ 2P2O5 là
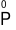 ⟶
⟶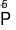 + 5e
+ 5e
Câu 14:
Hệ số cân bằng của H2 trong phản ứng Fe2O3 + H2⟶ Fe + H2O là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Sự thay đổi số oxi hóa của các nguyên tố: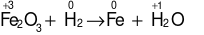
Quá trình oxi hóa và quá trình khử:
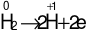
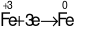
Áp dụng nguyên tắc: tổng số electron nhường bằng tổng số electron nhận
|
|
|
|
|
|
⇒
Fe2O3 + 3H2⟶ 2Fe + 3H2O
Câu 15:
Xác định hệ số cân bằng của HCl trong phản ứng dưới đây:
K2Cr2O7 + HCl ⟶ Cl2 + KCl + CrCl3 + H2O
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Sự thay đổi số oxi hóa của các nguyên tố:
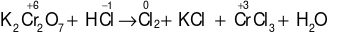
Quá trình oxi hóa và quá trình khử:


Áp dụng nguyên tắc: tổng số electron nhường bằng tổng số electron nhận
|
|
|
|
|
|
⇒ K2Cr2O7 + 14HCl ⟶3Cl2 + 2KCl + 2CrCl3 + 7H2O.