Giải Hóa học 10 Bài 9: Quy tắc octet
Mở đầu trang 49 Hóa học 10: Quan sát hiện tượng tự nhiên sau:
Viên bi rơi từ trên cao (vị trí có năng lượng cao hơn) xuống dưới đất (vị trí có năng lượng thấp hơn) mà không tự lăn theo chiều ngược lại.
Hãy cho biết quá trình trên diễn ra theo xu hướng tạo nên hệ bền hơn (năng lượng thấp hơn) hay kém bền hơn (năng lượng cao hơn).
Lời giải:
Quá trình trên diễn ra theo xu hướng tạo nên hệ bền hơn (năng lượng thấp hơn).
I. Quy tắc octet
Lời giải:
Na (Z = 11): 1s22s22p63s1
Cl (Z = 17): 1s22s22p63s23p5
Ne (Z = 10): 1s22s22p6
Ar (Z = 18): 1s22s22p63s23p6
Nguyên tử Ne (Z = 10) và Ar (Z = 18) có lớp electron ngoài cùng bền vững (lớp electron ngoài cùng đã bão hòa với 8 electron).
II. Vận dụng quy tắc octet trong quá trình hình thành liên kết hóa học của các nguyên tố nhóm A
Lời giải:
O (Z = 8) có cấu hình electron là 1s22s22p4
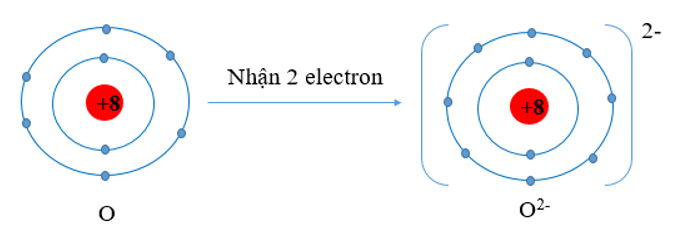
Oxygen có 6 electron lớp ngoài cùng. Vậy xu hướng cơ bản của nguyên tử oxygen khi hình thành liên kết hóa học là nhận thêm 2 electron để đạt được lớp vỏ có 8 electron ở lớp ngoài cùng như của khí hiếm Ne.
Sơ đồ nguyên tử O nhận thêm 2 electron vào lớp ngoài cùng:
Lời giải:
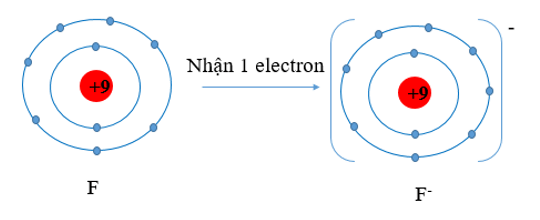
O và F đều có tính phi kim ⇒ Xu hướng cơ bản của nguyên tử O và F trong các phản ứng hóa học là nhận electron.
Trong đó O (Z = 8) có cấu hình electron là 1s22s22p4 ⇒ Nguyên tử O sẽ nhận thêm 2 electron để được lớp vỏ có 8 electron lớp ngoài cùng bền vững.
F (Z = 9) có cấu hình electron là 1s22s22p5 ⇒ Nguyên tử F sẽ nhận thêm 1 electron để được lớp vỏ có 8 electron lớp ngoài cùng bền vững.
a) K (Z = 19) và O (Z = 8)
b) Li (Z = 3) và F (Z = 9)
c) Mg (Z = 12) và P (Z = 15)
Lời giải:
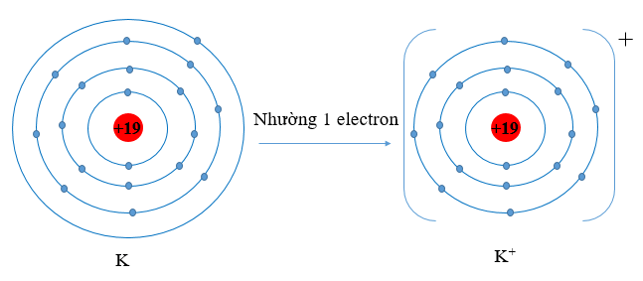
a) K (Z = 19) có cấu hình electron là: 1s22s22p63s23p64s1. Vậy K có 1 electron lớp vỏ ngoài cùng. Nguyên tử K có xu hướng nhường đi 1 electron để trở thành ion mang điện tích dương, kí hiệu là K+.
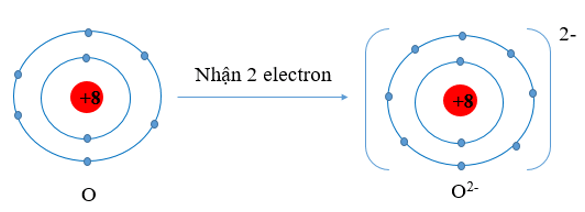
O (Z = 8) có cấu hình electron là 1s22s22p4. Vậy O có 6 electron lớp vỏ ngoài cùng nên nguyên tử O có xu hướng nhận thêm 2 electron để trở thành ion mang điện tích âm, kí hiệu là O2-
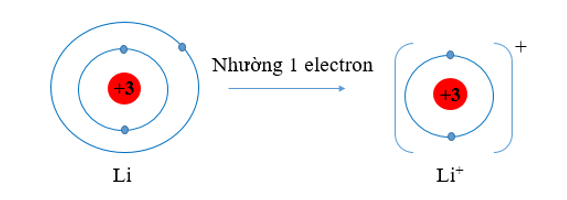
b) Li (Z = 3) có cấu hình electron là: 1s22s1. Vậy Li có 1 electron lớp vỏ ngoài cùng. Nguyên tử Li có xu hướng nhường đi 1 electron để trở thành ion mang điện tích dương, kí hiệu là Li+.
F (Z = 9) có cấu hình electron là: 1s22s22p5. Vậy F có 7 electron lớp vỏ ngoài cùng. Nguyên tử F có xu hướng nhận thêm 1 electron để trở thành ion mang điện tích âm, kí hiệu là F-.
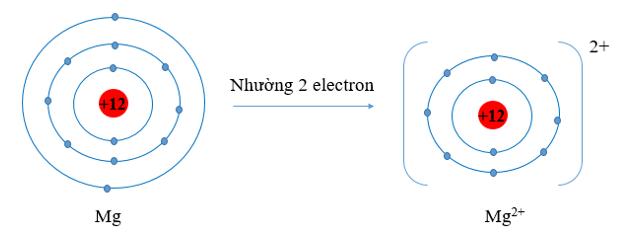
c) Mg (Z = 12) có cấu hình electron là: 1s22s22p63s2. Vậy Mg có 2 electron lớp vỏ ngoài cùng. Nguyên tử Mg có xu hướng nhường đi 2 electron để trở thành ion mang điện tích dương, kí hiệu là Mg2+.
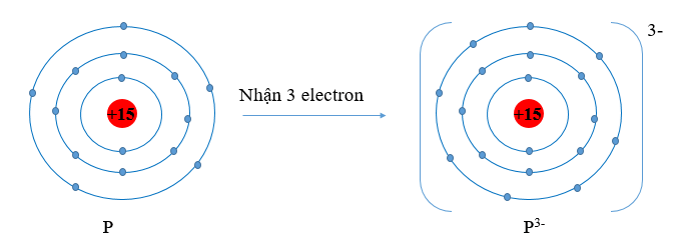
P (Z = 15) có cấu hình electron là: 1s22s22p63s23p3. Vậy P có 5 electron lớp vỏ ngoài cùng. Nguyên tử P có xu hướng nhận thêm 3 electron để trở thành ion mang điện tích âm, kí hiệu là P3-.
Lời giải:
Các nguyên tố thuộc chu kì 2, có 2 lớp electron. Lại có, lớp thứ 2 có 4 AO, mà mỗi AO có tối đa 2 electron nên các nguyên tố thuộc chu kì 2 chỉ có tối đa 8 electron.
Bài tập (trang 52)
A. Nhận 3 electron, nhường 3 electron.
B. Nhận 5 electron, nhường 5 electron.
C. Nhường 3 electron, nhận 3 electron.
D. Nhường 5 electron, nhận 5 electron.
Lời giải:
Đáp án đúng là: A
Nitrogen (Z = 7) có cấu hình electron là: 1s22s22p3
Lớp ngoài cùng của nguyên tử nitrogen có 5 electron, nên nguyên tử nitrogen có xu hướng nhận thêm 3 electron để đạt được cấu hình electron bền vững (8 electron ở lớp ngoài cùng).
Nhôm (Z = 13) có cấu hình electron là: 1s22s22p63s23p1
Lớp ngoài cùng của nguyên tử nhôm có 3 electron, nên nguyên tử nhôm có xu hướng nhường đi 3 electron để đạt được cấu hình electron bền vững (8 electron ở lớp ngoài cùng).
A. Boron
B. Potassium
C. Helium
D. Fluorine.
Lời giải:
Đáp án B
A. Boron (Z = 5): 1s22s22p1
Boron có 3 electron lớp ngoài cùng, là phi kim (trường hợp đặc biệt) nên không nhường electron.
B. Potassium (Z = 19): 1s22s22p63s23p64s1
Potassium có 1 electron lớp ngoài cùng nên có xu hướng nhường đi 1 electron này khi hình thành liên kết hóa học.
C. Helium (Z = 2): 1s2
Helium đã có cấu hình electron bền vững nên không nhường hoặc nhận electron.
D. Fluorine (Z = 9): 1s22s22p5
Fluorine có 7 electron lớp ngoài cùng nên có xu hướng nhận thêm 1 electron khi hình thành liên kết hóa học.
a) Kim loại điển hình tác dụng với phi kim điển hình.
b) Phi kim tác dụng với phi kim.
Lời giải:
a) Trong trường hợp kim loại điển hình tác dụng với phi kim điển hình, các nguyên tử kim loại sẽ có xu hướng nhường electron còn các nguyên tử phi kim sẽ có xu hướng nhận electron để hình thành liên kết hóa học.
b) Trong trường hợp phi kim tác dụng với phi kim, hai nguyên tử phi kim sẽ góp chung electron. Sau khi hình thành liên kết mỗi nguyên tử phi kim sẽ có 8 electron lớp ngoài cùng, giống lớp vỏ bền vững của khí hiếm.
Lời giải:
Ở dạng đơn chất, sodium (Na) có cấu hình electron là 1s22s22p63s1. Na có 1 electron lớp ngoài cùng. Nguyên tử Na dễ dàng nhường đi 1 electron để tạo thành ion Na+
Ở dạng đơn chất, chlorine (Cl) có cấu hình electron là 1s22s22p63s23p5. Cl có 7 electron lớp ngoài cùng. Nguyên tử Cl dễ dàng nhận thêm 1 electron để tạo thành ion Cl-.
Hai ion Na+ và Cl- hút nhau tạo thành hợp chất ion NaCl. Trong hợp chất ion NaCl cả Na+ và Cl- đều đã có cấu hình bền vững của khí hiếm nên không dễ dàng tham gia các phản ứng mà có sự nhường hoặc nhận electron.
Bài 5 trang 52 Hóa học 10: Cho một số hydrocarbon sau: H-C≡C-H, H2C=CH2 và H3C-CH3.
a) Những nguyên tử H và C nào trong các hydrocarbon trên thỏa mãn quy tắc octet?
Biết rằng mỗi gạch (-) trong các công thức trên biểu diễn hai electron hóa trị chung.
b) Một phân tử hydrocarbon có ba nguyên tử C và x nguyên tử H. Giá trị x lớn nhất có thể là bao nhiêu?
Lời giải:
a) Ta có, mỗi gạch trong các công thức H-C≡C-H, H2C=CH2 và H3C-CH3 biểu diễn hai electron hóa trị chung, do đó mỗi C đã đủ 8 electron ở lớp ngoài cùng; mỗi H đã đủ 2 electron ở lớp ngoài cùng (thõa mãn quy tắc octet).
b) Một phân tử hydrocarbon có ba nguyên tử C và x nguyên tử H.
Phân tử hydrocarbon có dạng: C3Hx
- Số các nguyên tử có hoá trị ≥ 2 là 3 (tức 3 C) ⇒ tổng số electron hoá trị là 3.4 = 12.
- Tổng số liên kết đơn giữa các nguyên tử có hoá trị ≥ 2 là: 3 – 1 = 2 ⇒ tổng số electron tham gia tạo liên kết là 2.2 = 4.
- Số H tối đa: x = 12 – 4 = 8.
Xem thêm lời giải bài tập SGK Hóa học lớp 10 Cánh diều hay, chi tiết khác: