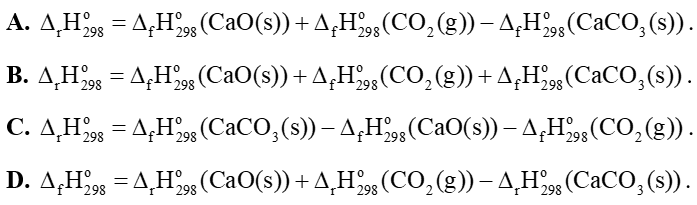Đề cương Học kì 2 Hóa học 10 Kết nối tri thức
I. Kiến thức ôn tập
1. Phản ứng oxi hóa - khử
- Khái niệm số oxi hóa và các quy tắc xác định số oxi hóa.
- Xác định được số oxi hóa của nguyên tố trong các phân tử đơn chất, hợp chất và ion.
- Khái niệm chất khử, chất oxi hóa, sự khử, sự oxi hóa và phản ứng oxi hóa - khử.
- Xác định được số electron nhường, nhận trong các phản ứng oxi hóa - khử và viết được quá trình khử, quá trình oxi hóa.
- Phân biệt được chất oxi hóa và chất khử, sự oxi hóa và sự khử trong phản ứng oxi hóa - khử cụ thể. - Lập được phương trình hóa học của phản ứng oxi hóa - khử (cân bằng theo phương pháp thăng bằng electron).
- Ý nghĩa của phản ứng oxi hóa - khử trong thực tiễn.
- Giải được các bài toán liên quan đến phản ứng oxi hóa - khử sử dụng định luật bảo toàn số mol electron.
2. Năng lượng hóa học
- Khái niệm phản ứng tỏa nhiệt và phản ứng thu nhiệt.
- Nhận biết một số phản ứng tỏa nhiệt và phản ứng thu nhiệt trong thực tiễn.
- Khái niệm biến thiên enthapy của phản ứng, biến thiên enthapy chuẩn và ý nghĩa của biến thiên enthapy.
- Khái niệm phương trình nhiệt hóa học của phản ứng.
- Khái niệm nhiệt tạo thành và nhiệt tạo thành chuẩn của một chất.
- Tính biến thiên enthapy của phản ứng dựa vào nhiệt tạo thành và năng lượng liên kết.
3. Tốc độ phản ứng
- Khái niệm tốc độ phản ứng hóa học, tốc độ trung bình của phản ứng.
- Viết được biểu thức và tính tốc độ trung bình của phản ứng theo chất phản ứng hoặc sản phẩm.
- Hiểu và giải thích được các yếu tố ảnh hưởng đến tốc độ phản ứng: nồng độ, áp suất, nhiệt độ, diện tích bề mặt tiếp xúc, chất xúc tác.
- Vận dụng được các yếu tố ảnh hưởng đến tốc độ phản ứng để làm tăng hoặc giảm tốc độ của một số phản ứng trong thực tế đời sống, sản xuất theo hướng có lợi.
- Giải được các bài toán về ảnh hưởng của nồng độ và nhiệt độ lên tốc độ phản ứng (quy tắc Van’t Hoff).
4. Nhóm halogen
- Vị trí nhóm halogen trong bảng tuần hoàn, cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố halogen và trạng thái tự nhiên của các halogen.
- Sự biến đổi độ âm điện, bán kính nguyên tử, tính phi kim của các nguyên tố trong nhóm từ fluorine đến iodine.
- Tính chất vật lý, sự biến đổi nhiệt độ nóng chảy và nhiệt độ sôi từ F2 đến I2.
- Tính chất hóa học cơ bản của các đơn chất halogen là tính oxi hóa mạnh, tính oxi hóa giảm dần từ F2 đến I2. Cl2, Br2, I2 ngoài tính oxi hóa còn có tính khử. Viết được phương trình hóa học chứng minh tính oxi hóa mạnh của các đơn chất halogen.
- Hiểu được tính tẩy màu của nước chlorine và nước Javel.
- Nguyên tắc và phương pháp điều chế Cl2 trong phòng thí nghiệm và trong công nghiệp - Tính chất vật lý và hóa học của các hydrogen halide, hydrohalic acid và muối halide.
- Quy luật biến đổi nhiệt độ sôi của các hydrohalic acid từ HF đến HI. - Quy luật biến đổi tính acid, tính khử của các hydrohalic acid.
- Ứng dụng của các hydrohalic acid, muối halide và phương pháp hóa học nhận biết ion halide.
- Giải được các bài toán về đơn chất halogen, hydrohalic acid và muối halide.
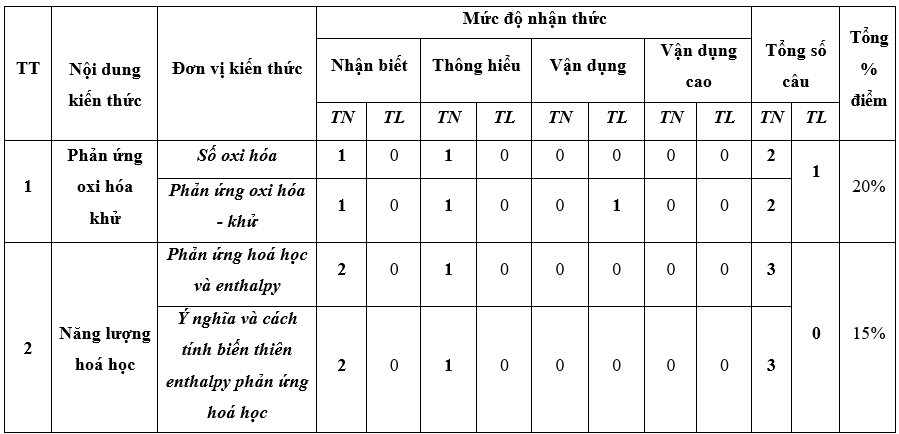
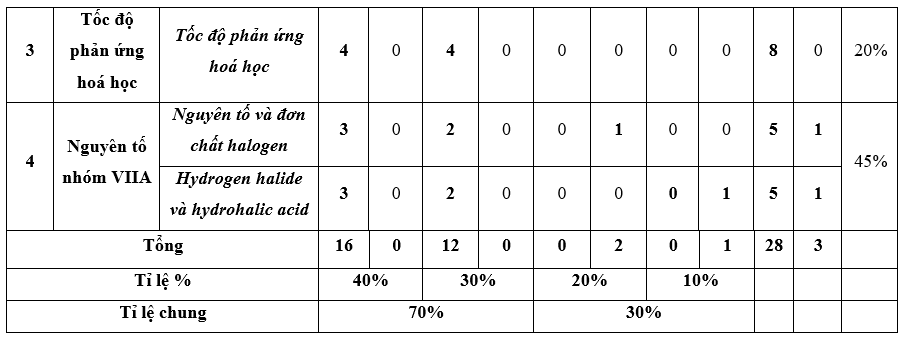
II. Ma trận đề thi
Ma trận đề kiểm tra cuối kì 2 - Hóa học 10 – Kết nối tri thức
III. Câu hỏi ôn tập
Xem chi tiết trong file đính kèm bên dưới
IV. Đề thi minh họa
Đề số 1
Phần I: Trắc nghiệm (7 điểm)
Câu 1: Số oxi hoá của Fe trong hợp chất Fe2O3 là
A. +2. B. +3.
C. -2. D. -3.
Câu 2: Hợp chất trong đó nitrogen có số oxi hoá -3 là
A. N2O. B. KNO3.
C. N2O3. D. NH4Cl.
Câu 3: Quá trình Ostwald dùng để sản xuất nitric acid từ ammonia được đề xuất vào năm 1902. Ở giai đoạn đầu của quá trình, ammonia bị oxi hoá bởi oxygen ở nhiệt độ cao khi có chất xúc tác:
4NH3 + 5O2 to→ 4NO + 6H2O
Chất bị oxi hoá trong quá trình trên là
A. NH3. B. O2.
C. NO. D. H2O.
Câu 4: Trong phản ứng oxi hoá – khử, chất khử là chất
A. nhận electron.
B. nhường proton.
C. nhường electron.
D. nhận neutron.
Câu 5: Phản ứng nào sau đây là phản ứng thu nhiệt?
A. Phản ứng đốt cháy than trong không khí.
B. Phản ứng tạo gỉ sắt.
C. Phản ứng oxi hóa glucose trong cơ thể.
D. Phản ứng trong lò nung clinker xi măng.
Câu 6: Phản ứng đốt cháy hoàn toàn 1 mol carbon graphite trong khí oxygen dư (ở điều kiện chuẩn) tạo ra 1 mol CO2, nhiệt lượng toả ra là 393,5 kJ. Nhiệt tạo thành chuẩn của CO2(g) là
A. + 393,5 kJ/ mol.
B. –393,5 kJ/ mol.
C. +196,75 kJ/ mol.
D. –196,75 kJ/ mol.
Câu 7: Enthalpy tạo thành chuẩn của một đơn chất bền là
A. biến thiên enthalpy chuẩn của phản ứng giữa đơn chất đó với hydrogen.
B. là biến thiên enthalpy chuẩn của phản ứng giữa đơn chất đó với oxygen.
C. bằng 0.
D. được xác định từ nhiệt độ nóng chảy của nguyên tố đó.
Câu 8: Cho phương trình nhiệt hóa học của phản ứng:
N2(g)+O2(g)→t°
Nhận xét nào sau đây là đúng?
A. Phản ứng tỏa nhiệt mạnh.
B. Phản ứng xảy ra thuận lợi ở điều kiện thường.
C. Phản ứng xảy ra dưới điều kiện nhiệt độ thấp.
D. Phản ứng thu nhiệt.
Câu 9: Cho phản ứng sau: CaCO3(s) → CaO(s) + CO2(g)
Biến thiên enthalpy chuẩn của phản ứng được tính theo công thức là
Câu 10: Cho phản ứng tạo thành propene từ propyne:
Cho giá trị trung bình của các năng lượng liên kết ở điều kiện chuẩn:
|
Liên kết |
C – H |
C – C |
C = C |
C ≡ C |
H - H |
|
Eb (kJ/mol) |
413 |
347 |
614 |
839 |
432 |
Biến thiên enthalpy chuẩn của phản ứng là
A. -169 kJ.
B. +169 kJ.
C. -196 kJ.
D. +196 kJ.
Câu 11: Sự thay đổi lượng chất trong khoảng thời gian vô cùng ngắn được gọi là
A. tốc độ phản ứng hoá học.
B. tốc độ trung bình của phản ứng.
C. tốc độ tức thời của phản ứng.
D. vận tốc trung bình của phản ứng.
Câu 12: Cho phương trình phản ứng tổng quát sau: 2A + B → C.
Tốc độ phản ứng tại một thời điểm được tính bằng biểu thức:.
Hằng số tốc độ k phụ thuộc vào yếu tố nào sau đây?
A. Nồng độ của chất.
B. Nồng độ của chất B.
C. Nhiệt độ của phản ứng.
D. Thời gian xảy ra phản ứng.
Câu 13: Cho bột Fe vào dung dịch HCl loãng. Sau đó đun nóng hỗn hợp này. Phát biểu nào sau đây không đúng?
A. Khí H2 thoát ra nhanh hơn.
B. Bột Fe tan nhanh hơn.
C. Lượng muối thu được nhiều hơn.
D. Nồng độ HCl giảm nhanh hơn.
Câu 14: Khí oxygen được điều chế trong phòng thí nghiệm bằng cách nhiệt phân potassium chlorate với xúc tác manganes dioxide. Để thí nghiệm thành công và rút ngắn thời gian tiến hành có thể dùng một số biện pháp sau:
(1) Trộn đều bột potassium chlorate và xúc tác.
(2) Nung ở nhiệt độ cao.
(3) Dùng phương pháp dời nước để thu khí oxygen.
(4) Nghiền nhỏ potassium chlorate.
Số biện pháp dùng để tăng tốc độ phản ứng là
A. 2. B. 3.
C. 4. D. 5.
Câu 15: Hydrogen peroxide phân hủy theo phản ứng sau: 2H2O2 → 2H2O + O2.
Tại thời điểm ban đầu, thể tích khí oxygen là 0 cm3, sau thời gian 15 phút thể tích khí oxygen là 16 cm3. Tốc độ trung bình của phản ứng trong 15 phút đầu tiên là
A. 1,067 M/ s.
B. 1,067 M/ phút.
C. 1,067 cm3/ s.
D. 1,067 cm3/ phút.
Câu 16: Ở 35oC, phản ứng có tốc độ là 0,036 mol/ (L.h); ở 45oC, phản ứng có tốc độ là 0,09 mol/ (L.h). Hệ số nhiệt độ γ của phản ứng là
A. 1,5. B. 2.
C. 2,5. D. 3.
Câu 17: Cho phản ứng đơn giản sau (xảy ra trong bình kín):
2NO(g) + O2(g) → 2NO2(g)
Ở nhiệt độ không đổi, nồng độ NO tăng hai lần, nồng độ O2 không đổi thì
A. tốc độ phản ứng không thay đổi.
B. tốc độ phản ứng tăng 2 lần.
C. tốc độ phản ứng tăng 4 lần.
D. tốc độ phản ứng giảm 2 lần.
Câu 18: Nhận xét nào sau đây là sai?
A. Khi nồng độ chất tan trong dung dịch tăng, tốc độ phản ứng tăng.
B. Với mọi phản ứng, khi tăng áp suất, tốc độ phản ứng tăng.
C. Chất xúc tác làm tăng tốc độ phản ứng.
D. Đối với phản ứng có sự tham gia của chất khí, khi áp suất tăng, tốc độ phản ứng tăng.
Câu 19: Trong bảng tuần hoàn các nguyên tố hóa học, các nguyên tố halogen thuộc nhóm
A. IA. B. IIA.
C. VIIA. D. VIIIA.
Câu 20: Halogen nào được dùng trong sản xuất nhựa Teflon?
A. Chlorine.
B. Iodine.
C. Fluorine.
D. Bromine.
Câu 21: Trong phản ứng hóa học sau: SO2 + Br2 + 2H2O → 2HBr + H2SO4. Bromine đóng vai trò
A. chất khử.
B. vừa là chất oxi hóa, vừa là chất khử.
C. chất oxi hóa.
D. không là chất oxi hóa, không là chất khử.
Câu 22: Cho các phản ứng hóa học sau, phản ứng nào chứng minh Cl2 có tính oxi hoá mạnh hơn Br2?
A. Br2 + 2NaCl → 2NaBr + Cl2.
B. Cl2 + 2NaOH → NaCl + NaClO + H2O.
C. Br2 + 2NaOH → NaBr + NaBrO + H2O.
D. Cl2 + 2NaBr → 2NaCl + Br2.
Câu 23: Phương trình hóa học nào sau đây viết sai?
A. Br2 + Cu → CuBr2.
B. 2HCl + Na2CO3 → 2NaCl + CO2 + H2O.
C. NaBr + AgNO3 → AgBr + NaNO3.
D. Cl2 + Fe → FeCl2.
Câu 24: Nguyên nhân dẫn tới nhiệt độ nóng chảy, nhiệt độ sôi của các đơn chất halogen tăng từ fluorine đến iodine là do từ fluorine đến iodine,
A. khối lượng phân tử và tương tác van der Walls đều tăng.
B. tính phi kim giảm và tương tác van der Walls tăng.
C. khối lượng phân tử tăng và tương tác van der Walls giảm.
D. độ âm điện và tương tác van der Walls tăng giảm.
Câu 25: Phát biểu nào sau đây không đúng?
A. Trong các hợp chất, ngoài số oxi hoá –1, fluorine còn có các số oxi hoá +1, +3, +5, +7.
B. Muối AgI không tan trong nước, muối AgF tan trong nước.
C. Fluorine có tính oxi hóa mạnh hơn chlorine.
D. Dung dịch HF hòa tan được SiO2.
Câu 26: Cho lượng dư dung dịch AgNO3 tác dụng với 100 ml dung dịch hỗn hợp NaF 0,05M và NaCl 0,1M. Khối lượng kết tủa thu được là
A. 1,345 gam.
B. 3,345 gam.
C. 2,875 gam.
D. 1,435 gam.
Câu 27: Cho 10 gam CaCO3 tác dụng hết với dung dịch HCl dư, thu được V lít khí CO2 (đkc). Giá trị của V là
A. 2,24 L. B. 2,479 L.
C. 3,36 L. D. 3,719 L.
Câu 28: Nhỏ vài giọt dung dịch nào sau đây vào dung dịch AgNO3 thu được kết tủa màu vàng nhạt.
A. HCl. B. NaBr.
C. NaCl. D. HF.
Phần II: Tự luận
Câu 1 (1 điểm): Hãy viết phương trình hóa học để chứng minh chlorine có tính oxi hóa mạnh hơn bromine.
Câu 2 (1 điểm): Cho sodium iodide (NaI) tác dụng với potassium permanganate (KMnO4) trong dung dịch sulfuric acid (H2SO4) thu được 3,02 gam manganese(II) sulfate (MnSO4), I2; K2SO4 và Na2SO4.
a) Viết phương trình hoá học xảy ra, chỉ rõ chất khử, chất oxi hoá, quá trình khử, quá trình oxi hoá.
b) Tính khối lượng I2 tạo thành.
Câu 3 (1 điểm): Bằng phương pháp hóa học, hãy phân biệt các dung dịch sau chứa trong các lọ riêng biệt mất nhãn: HCl, NaCl, NaI.
Xem thêm các đề cương, đề thi Hóa học 10 Kết nối tri thức hay, chi tiết khác: